题目内容
在实验室利用一氧化碳还原氧化铜制取铜并生成二氧化碳:CO+CuO  Cu+CO2。若制取3.2 g铜,需要氧化铜的质量是多少?同时生成二氧化碳的体积是多少?(二氧化碳的密度为1. 96 g/L,计算二氧化碳的体积精确到0. 01 L)
Cu+CO2。若制取3.2 g铜,需要氧化铜的质量是多少?同时生成二氧化碳的体积是多少?(二氧化碳的密度为1. 96 g/L,计算二氧化碳的体积精确到0. 01 L)
 Cu+CO2。若制取3.2 g铜,需要氧化铜的质量是多少?同时生成二氧化碳的体积是多少?(二氧化碳的密度为1. 96 g/L,计算二氧化碳的体积精确到0. 01 L)
Cu+CO2。若制取3.2 g铜,需要氧化铜的质量是多少?同时生成二氧化碳的体积是多少?(二氧化碳的密度为1. 96 g/L,计算二氧化碳的体积精确到0. 01 L)解:设需要氧化铜的质量为x,生成二氧化碳的质量为 y,则:
CO+CuO Cu+ CO2
Cu+ CO2
80 64 44
x 3.2g y,
 解得x=4 g,
解得x=4 g,
 解得y=2.2 g
解得y=2.2 g
故二氧化碳的体积为 =1.12 L
=1.12 L
答:需要氧化铜的质量为4 g,同时生成二氧化碳的体积为1. 12 L。
CO+CuO
 Cu+ CO2
Cu+ CO2 80 64 44
x 3.2g y,
 解得x=4 g,
解得x=4 g, 解得y=2.2 g
解得y=2.2 g故二氧化碳的体积为
 =1.12 L
=1.12 L答:需要氧化铜的质量为4 g,同时生成二氧化碳的体积为1. 12 L。

练习册系列答案
相关题目


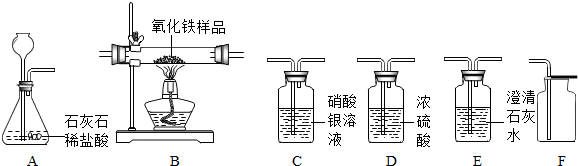
 (2003?宿迁)某学生在报刊上看到:孔雀石(主要成份为Cu2(OH)2CO3,假设其它成份不参加反应)在熊熊燃烧的木碳上灼烧后,灰烬中有红色固体生成.他想在实验室利用右图装置来验证此现象,将少量孔雀石和木碳粉放入试管,然后加热.试回答下列问题
(2003?宿迁)某学生在报刊上看到:孔雀石(主要成份为Cu2(OH)2CO3,假设其它成份不参加反应)在熊熊燃烧的木碳上灼烧后,灰烬中有红色固体生成.他想在实验室利用右图装置来验证此现象,将少量孔雀石和木碳粉放入试管,然后加热.试回答下列问题