题目内容
2.测定粗盐(含难溶杂质)中氯化钠质量分数的实验,操作步骤如下,填空.(1)称量.将粗盐样品10g放在托盘天平的左盘上.
(2)溶解.将称取的粗盐溶于适量蒸馏水,溶解操作应在烧杯(填仪器名称)里进行,并用玻璃棒搅拌,其目的是搅拌,加快溶解速率.
(3)过滤.过滤时,玻璃棒的作用是引流.
(4)蒸发.加热蒸发滤液并用玻璃棒不断搅拌,其目的是防止局部温度过高,造成液体飞溅.
(5)计算.把固体转移到纸上并用托盘天平称量,测得纯净的氯化钠固体8.9g,则粗盐中氯化钠的质量分数(即精盐的产率)为89%.
分析 (2)根据溶解操作的方法,进行分析解答.
(3)根据过滤时玻璃棒的作用,进行分析解答.
(4)根据蒸发操作中玻璃棒的作用,进行分析解答.
(5)根据精盐的产率=$\frac{精盐的质量}{粗盐的质量}$×100%,进行分析解答.
解答 解:(2)溶解操作应在烧杯中进行,并用玻璃棒搅拌,其目的是搅拌,加快溶解速率.
(3)过滤时玻璃棒的作用是引流.
(4)加热蒸发滤液并用玻璃棒不断搅拌,其目的是防止局部温度过高,造成液体飞溅.
(5)测得纯净的氯化钠固体8.9g,则粗盐中氯化钠的质量分数(即精盐的产率)为$\frac{8.9g}{10g}$×100%=89%.
故答案为:(2)烧杯;搅拌,加快溶解速率;(3)引流;(4)防止局部温度过高,造成液体飞溅;(5)89%.
点评 本题难度不大,掌握粗盐提纯的原理、实验步骤(溶解、过滤、蒸发)、注意事项是正确解答本题的关键.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
15.家庭装修中使用的夹芯板、地板、家具都可能释放出甲醛(CH2O),它是室内污染物之一.纳米二氧化钛(TiO2)可使吸附在其表面的甲醛等物质发生氧化,从而降低空气中有害物质的浓度.正钛酸(H4TiO4)在一定条件下分解失水可制得纳米二氧化钛.下列说法不正确的是( )
| A. | 纳米TiO2属于氧化物 | |
| B. | 甲醛由碳、氢、氧原子构成 | |
| C. | 纳米TiO2添加到墙面涂料中,可有效净化空气中的甲醛 | |
| D. | 制备纳米TiO2的反应:H4TiO4$\frac{\underline{\;一定条件\;}}{\;}$TiO2+2H2O |

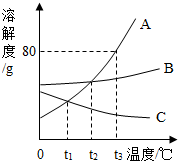 如图是A、B、C三种物质的溶解度随温度变化的曲线图,据图回答下列问题.
如图是A、B、C三种物质的溶解度随温度变化的曲线图,据图回答下列问题.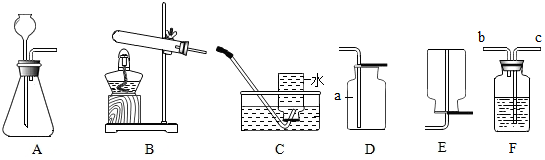
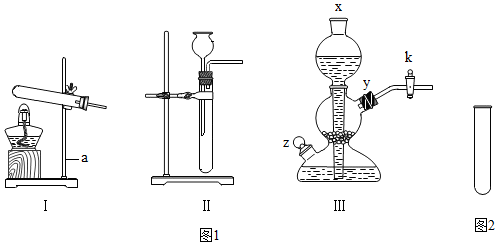
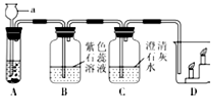 同学们在实验室中制取二氧化碳,探究二氧化碳性质的装置图如图:
同学们在实验室中制取二氧化碳,探究二氧化碳性质的装置图如图: