题目内容
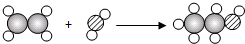 如图是工业上在一定条件下制取乙醇的反应微观示意图:(“
如图是工业上在一定条件下制取乙醇的反应微观示意图:(“ ”代表氢原子,“
”代表氢原子,“ ”代表碳原子,“
”代表碳原子,“ ”代表氧原子)根据微观图示,可知下列选项错误的( )
”代表氧原子)根据微观图示,可知下列选项错误的( )A.该反应属于化合反应
B.氧原子体积小于碳原子体积
C.化学反应中分子、原子都不可分
D.C2H4+H2O=C2H5OH
【答案】分析:A、根据化合反应的特点‘多合一’,并结合图示分析解答;
B、根据氧原子和碳原子的质子数、电子层数分析解答;
C、依据微观示意图分析解答;
D、根据反应的微观示意图,分析反应物、生成物及反应条件,写出反应的方程式.
解答:解:A、由图示可知,该反应是由两种物质生成一种物质,属于化合反应,正确;
B、氧原子和碳原子电子层数一样多,而核内质子数氧的多,因而对外层电子的引力大,电子和质子距离近,则原子的半径小,对应体积小,故碳原子的体积比氧原子的体积大,正确;
C、通过微观图可知:该反应中分子划分为原子,然后原子重新组合成新分子,原子在反应前后不变,故说法错误;
D、由图示可知物质的分子构成,写出反应的方程式是C2H4+H2O=C2H5OH,正确;
故选C.
点评:能通过反应的微观示意图,判断出物质的构成,反应的特点等,是解决此题目的关键所在.
B、根据氧原子和碳原子的质子数、电子层数分析解答;
C、依据微观示意图分析解答;
D、根据反应的微观示意图,分析反应物、生成物及反应条件,写出反应的方程式.
解答:解:A、由图示可知,该反应是由两种物质生成一种物质,属于化合反应,正确;
B、氧原子和碳原子电子层数一样多,而核内质子数氧的多,因而对外层电子的引力大,电子和质子距离近,则原子的半径小,对应体积小,故碳原子的体积比氧原子的体积大,正确;
C、通过微观图可知:该反应中分子划分为原子,然后原子重新组合成新分子,原子在反应前后不变,故说法错误;
D、由图示可知物质的分子构成,写出反应的方程式是C2H4+H2O=C2H5OH,正确;
故选C.
点评:能通过反应的微观示意图,判断出物质的构成,反应的特点等,是解决此题目的关键所在.

练习册系列答案
相关题目

 (1)用CO合成甲醇的反应为:CO(g)+2H2(g)
(1)用CO合成甲醇的反应为:CO(g)+2H2(g)  CH3OH (g)
CH3OH (g) CH3OH+H2O。
CH3OH+H2O。
 ②为探究用CO2生产燃料甲醇的反应原理,现进行如下实验:在一恒温恒容密闭容器中,充入1molCO2 和3molH2,进行上述反应。测得CO2。
②为探究用CO2生产燃料甲醇的反应原理,现进行如下实验:在一恒温恒容密闭容器中,充入1molCO2 和3molH2,进行上述反应。测得CO2。 ①甲醇蒸汽重整法。主要反应为;CH3OH(g)
①甲醇蒸汽重整法。主要反应为;CH3OH(g)