题目内容
煤是重要的化工原料,用煤作燃料,不仅是极大的浪费,而且因煤中含有硫的化合物(如FeS2),燃烧时会生成SO2气体造成环境污染。若煤中含FeS25%,燃烧时有90%的硫的化合物转化为二氧化硫被排放入大气之中。燃烧时化学反应方程式为:  。
。
(1)我国计划从2003年至2007年,将SO2的排放量从1995万吨降到1800万吨,意味着2007年比2003年应少燃烧这种煤多少万吨?
(2)若以SO2形成硫酸酸雨计算,2007年雨水中减少排放硫酸多少万吨?
 。
。 (1)我国计划从2003年至2007年,将SO2的排放量从1995万吨降到1800万吨,意味着2007年比2003年应少燃烧这种煤多少万吨?
(2)若以SO2形成硫酸酸雨计算,2007年雨水中减少排放硫酸多少万吨?
解:(1)设2007年比2003年少燃烧这种煤的质量为x,则有:

4×120 8×64
x×5%×90% (1995 - 1800)万吨=195万吨
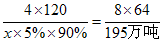 ,x=4062.5万吨
,x=4062.5万吨
(2)设2007年雨水中减少排放硫酸的质量为y,则有:
SO2 ~ H2SO4
64 98
195万吨 y
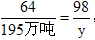 ,y= 298.6万吨
,y= 298.6万吨

4×120 8×64
x×5%×90% (1995 - 1800)万吨=195万吨
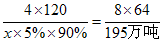 ,x=4062.5万吨
,x=4062.5万吨 (2)设2007年雨水中减少排放硫酸的质量为y,则有:
SO2 ~ H2SO4
64 98
195万吨 y
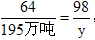 ,y= 298.6万吨
,y= 298.6万吨
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 煤是重要的化工原料,用煤作燃料不仅是极大的浪费,而且固全煤中含有的硫,在燃烧时生二氧化硫气体,造成环境污染.我省某市冬季取暖约150天,每天消耗含硫1%的煤200吨.
煤是重要的化工原料,用煤作燃料不仅是极大的浪费,而且固全煤中含有的硫,在燃烧时生二氧化硫气体,造成环境污染.我省某市冬季取暖约150天,每天消耗含硫1%的煤200吨.