题目内容
亚硝酸钠(NaNO2)是一种亚硝酸盐;如果食物中亚硝酸盐含量较高会引起食物中毒.其中毒症状是,1-3小时内便可让人缺氧,出现恶心、呕吐、头晕、乏力、口唇发紫、呼吸困难.请根据要求回答下面的问题.a.NaNO2中氮元素的化合价是 ;
b.NaNO2中氮,氧元素的质量比是 ;钠元素的质量分数是 (保留一位小数);
c.欲配置140g的2%亚硝酸钠溶液用于亚硝酸钠的毒性实验;那么需要NaNO2 g;水 g.
【答案】分析:a、根据在化合物中正负化合价代数和为零,结合NaNO2的化学式进行解答本题.
b、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,根据化合物中元素的质量分数= ×100%,进行分析解答.
×100%,进行分析解答.
c、根据溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量-溶质质量,进行分析计算.
解答:解:a、钠元素显+1,氧元素显-2,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可知NaNO2中氮元素的化合价:(+1)+x+(-2)×2=0,则x=+3.
b、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,NaNO2中氮,氧元素的质量比是(14×1):(16×2)=7:16;
根据化合物中元素的质量分数= ×100%,钠元素的质量分数是
×100%,钠元素的质量分数是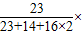 100%=33.3%.
100%=33.3%.
c、配置140g的2%亚硝酸钠溶液,需要NaNO2的质量为140g×2%=28g,需要水的质量为:140g-28g=112g.
故答案为:a、+3;b、7:16;33.3%;c、28;112.
点评:本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、化学式的有关计算、溶质质量分数的有关计算等是正确解答本题的关键.
b、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,根据化合物中元素的质量分数=
 ×100%,进行分析解答.
×100%,进行分析解答.c、根据溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量-溶质质量,进行分析计算.
解答:解:a、钠元素显+1,氧元素显-2,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可知NaNO2中氮元素的化合价:(+1)+x+(-2)×2=0,则x=+3.
b、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,NaNO2中氮,氧元素的质量比是(14×1):(16×2)=7:16;
根据化合物中元素的质量分数=
 ×100%,钠元素的质量分数是
×100%,钠元素的质量分数是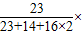 100%=33.3%.
100%=33.3%.c、配置140g的2%亚硝酸钠溶液,需要NaNO2的质量为140g×2%=28g,需要水的质量为:140g-28g=112g.
故答案为:a、+3;b、7:16;33.3%;c、28;112.
点评:本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、化学式的有关计算、溶质质量分数的有关计算等是正确解答本题的关键.

练习册系列答案
相关题目
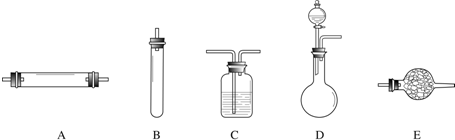
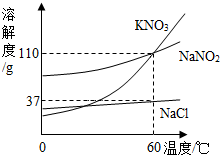 (2013?历下区二模)亚硝酸钠(NaNO2)常用作食品的发色剂和防腐剂,但食品中的亚硝酸钠含量超标会危害人体健康.亚硝酸钠具有咸味,外形和食盐很相似,亚硝酸钠的水溶液呈碱性.建筑行业常用亚硝酸钠作水泥添加剂,近年来,在建筑工地多次发生误将亚硝酸钠当作食盐食用导致中毒的事件.
(2013?历下区二模)亚硝酸钠(NaNO2)常用作食品的发色剂和防腐剂,但食品中的亚硝酸钠含量超标会危害人体健康.亚硝酸钠具有咸味,外形和食盐很相似,亚硝酸钠的水溶液呈碱性.建筑行业常用亚硝酸钠作水泥添加剂,近年来,在建筑工地多次发生误将亚硝酸钠当作食盐食用导致中毒的事件.