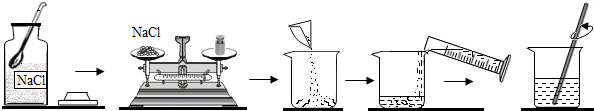
题目内容
11.在自来水消毒过程中通常要发生化学反应,其反应的微观过程如图所示.
请根据以上反应,结合所学知识,写出你获得的信息(至少写2条)
(1)该反应的方程式为H2O+Cl2═HCl+HClO
(2)反应前后原子的种类和数目没有改变或反应前后分子的种类发生了改变等.
分析 根据反应的模型图及物质的微观构成模型图可知反应物是氯气和水,生成物是盐酸和次氯酸,通过比较分子、原子在化学反应前后原子的种类与数量的特点、化学反应的实质等进行分析回答.
解答 解:通过反应的模型图及物质的微观构成模型图可知:①反应物是氯气和水,生成物是盐酸和次氯酸,各物质的微粒个数关系是1:1:1:1,所以反应的方程式为H2O+Cl2═HCl+HClO;②从图中可以看出:反应前有一个氧原子、两个氢原子、两个氯原子,反应后也有一个氧原子、两个氢原子、两个氯原子,反应前后原子的种类和数目没有改变;③反应前后分子的种类发生了改变等;
故答案为:(1)该反应的方程式为H2O+Cl2═HCl+HClO;(2)反应前后原子的种类和数目没有改变或反应前后分子的种类发生了改变等.
点评 本题主要考查了学生观察、分析微观粒子模型图的能力及对反应实质的认识,解答时弄清微观粒子的构成,并把微观粒子与宏观物质联系起来是解答的关键.

练习册系列答案
相关题目
2.某物质经测定只含有一种元素,则关于该物质说法正确的是( )
| A. | 一定是单质 | B. | 一定不是化合物 | C. | 一定是混合物 | D. | 一定不是纯净物 |
19.从下列图片中不能获取的信息是( )


| A. | 分子之间有间隔 | |
| B. | 构成物质的粒子有分子、原子和离子 | |
| C. | 硅原子是由原子核和电子构成的 | |
| D. | 受热水分子运动速率加快 |
16.研究物质时,常常先把物质进行分类.下列物质中属于纯净物的是( )
| A. | 清新的空气 | B. | 黄泥水 | C. | 纯净的食盐水 | D. | 蒸馏水 |
3.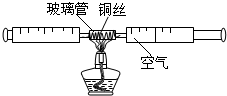 在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的硬质玻璃管加热,同时缓慢推动两个注射器活塞,过一段时间后停止加热,待冷却至室温后,将气体全部推至一支注射器内,读出注射器内气体的体积.
在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的硬质玻璃管加热,同时缓慢推动两个注射器活塞,过一段时间后停止加热,待冷却至室温后,将气体全部推至一支注射器内,读出注射器内气体的体积.
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是使氧气与铜充分反应.
(2)写出该实验中硬质玻璃管里出现的现象:红色铜逐渐变成黑色,发生化学反应的文字表达式:铜+氧气$\stackrel{加热}{→}$氧化铜,反应基本类型是化合反应.
(3)小强测得实验结果如下:
由此数据可以推算出他测定的空气中氧气的体积分数小于 2l%(填“大于”或“等于”或“小于”).造成该实验出现误差的原因可能是①②③(填序号).
①交替缓缓推动两个注射器活塞次数较少;②读数时没有冷却至室温;③加入铜丝量太少;④加入铜丝量太多.
(4)通过上面的实验,你学到的测量混合物中某成分含量的方法是通过化学反应除去混合物中的一种成分,再测量混合物在反应前后体积(或质量)的变化,从而得出该种成分的含量.
 在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的硬质玻璃管加热,同时缓慢推动两个注射器活塞,过一段时间后停止加热,待冷却至室温后,将气体全部推至一支注射器内,读出注射器内气体的体积.
在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的硬质玻璃管加热,同时缓慢推动两个注射器活塞,过一段时间后停止加热,待冷却至室温后,将气体全部推至一支注射器内,读出注射器内气体的体积.(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是使氧气与铜充分反应.
(2)写出该实验中硬质玻璃管里出现的现象:红色铜逐渐变成黑色,发生化学反应的文字表达式:铜+氧气$\stackrel{加热}{→}$氧化铜,反应基本类型是化合反应.
(3)小强测得实验结果如下:
| 反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
| 25mL | 22mL |
①交替缓缓推动两个注射器活塞次数较少;②读数时没有冷却至室温;③加入铜丝量太少;④加入铜丝量太多.
(4)通过上面的实验,你学到的测量混合物中某成分含量的方法是通过化学反应除去混合物中的一种成分,再测量混合物在反应前后体积(或质量)的变化,从而得出该种成分的含量.
1.空气中含量较多且化学性质比较活泼的气体是( )
| A. | O2 | B. | N2 | C. | 稀有气体 | D. | CO2 |