题目内容
高锰酸钾在生产、生活中有广泛应用。实验小组对高锰酸钾的某些性质进行研究。
Ⅰ.不稳定性
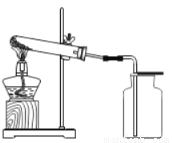
(1)如图所示进行实验,受热分解的文字表达式为___________________________
(2)用向上排空气法收集O2的原因是_______________________________________
(3)用排水法收集O2时,实验结束后先熄灭酒精灯,导致水槽中水倒流进入了导气管。可采取的补救措施是_____________________________________________(说出一种)
Ⅱ.腐蚀性:“对比试验”是科学探究常用的方法
(查阅资料)KMnO4溶液有腐蚀性
(进行实验)在室温下,将铜片分别浸泡在4种浸泡相同时间,现象如下表:
编号 | ① | ② | ③ | ④ | |
实验 |
25mL 0.1% KMnO4溶液 |
25mL 0.1%KMnO4溶 液+10滴浓硫酸 |
25mL蒸馏水+ 10滴浓硫酸 |
25mL 1% KMnO4溶 液+10滴浓硫酸 | |
铜片 质量/g | 实验前 | 0.54 | 0.54 | 0.54 | 0.54 |
18小时后 | 0.54 | 0.52 | X | 0.43 |
(解释与结论)
(4)通过对比②和④,得出的结论是____________________________________
(5)实验③中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,X的值为_______,需要对比___(填编号)
(6)为了探究KMnO4的腐蚀性是否与温度有关,请您补充探究实验⑤_______________________
工业上生产电石(CaC2)并制备重要工业原料乙炔(CxHy)流程如图1所示:
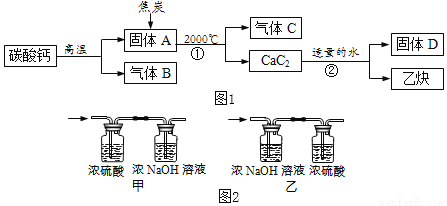
【资料】
①碳酸钙高温分解可得两种氧化物。
②浓硫酸具有强吸水性,NaOH溶液能吸收CO2。
【讨论】
(1)C、B组成元素相同,C有毒,反应①化学方程式为_____。
(2)D微溶于水,溶解度随温度升高而减小,D的化学式是_____。
【测定乙炔组成】
资料:一个乙炔分子有四个原子构成。
(3)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过如图2所示的_____(选填“甲”或“乙”)装置,并再缓缓通一段时间的N2,并记录实验数据于如表中。
装置 | 反应前质量 | 反应后质量 |
浓硫酸 | 125.3g | 127.1g |
浓NaOH溶液 | 78.2g | 87.0g |
(4)实验中“缓缓通一段时间的N2”的目的是_____。
(5)计算:乙炔中碳元素质量为_____g,氢元素质量为_____g,乙炔化学式为_____。
(6)反应②的化学方程式为_____。








 点燃酒精灯 B.
点燃酒精灯 B.  过滤
过滤 量取5.5mL液体 D.
量取5.5mL液体 D.  称量10.05g固体
称量10.05g固体