题目内容
依据质量守恒定律,12g碳和40g氧气充分反应,生成52g二氧化碳,对吗?
答案:
解析:
解析:
|
解答:表面上,根据质量守恒定律,12g碳和40g氧气反应,生成52g二氧化碳.但需要注意的是,必须是参加反应的各物质的质量总和才等于生成物的质量总和,不要把没有参加反应的物质的质量计算到反应物质量总和之中.需要判断给的物质是否都反应了.本题中的12g碳和40g氧气反应,并不是12g碳和40g氧气恰好反应,事实上,12g碳跟32g氧气恰好完全反应,题目提供的40g氧气只有32g氧气参加了反应,因此有(40g-32g)=8g氧气没有参加反应.根据质量守恒定律,参加反应的各物质的质量总和才等于生成物的质量总和,得到等式: 参加反应的碳的质量+参加反应的氧气的质量=生成的二氧化碳的质量 12g+32g=生成的二氧化碳的质量 生成的二氧化碳的质量=44g,而不是12g+40g=52g二氧化碳. |

练习册系列答案
相关题目
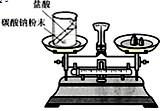 26、请根据题目要求回答下列问题.
26、请根据题目要求回答下列问题.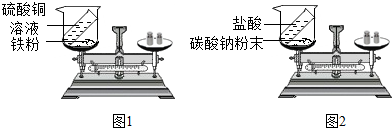
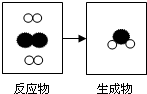 如图是密闭体系中某反应的微观示意图,“
如图是密闭体系中某反应的微观示意图,“ ”和“
”和“ ”分别表示不同原子.请用下列粒子的字母序号回答(1)、(2)两个小题:
”分别表示不同原子.请用下列粒子的字母序号回答(1)、(2)两个小题: