题目内容
19.用20mL质量分数为70%的硫酸溶液(密度为1.6g/cm3),以配制质量分数为28%的硫酸溶液(密度为1.2g/cm3),下列仪器中①烧杯②滴管③漏斗④量筒⑤玻璃棒⑥天平⑦酒精灯,需要用到的是( )| A. | ②④⑥⑦ | B. | ①②④⑤ | C. | ①③⑤⑦ | D. | ①③④⑥ |
分析 用20mL质量分数为70%的硫酸溶液(密度为1.6g/cm3),配制质量分数为28%的硫酸溶液,采用的是将浓溶液加水稀释的方法,由配制的步骤分析判断需要的仪器.
解答 解:用20mL质量分数为70%的硫酸溶液(密度为1.6g/cm3),配制质量分数为28%的硫酸溶液,采用的是将浓溶液加水稀释的方法,首先计算配制溶液所需70%的硫酸溶液和水的质量,再量取所需的70%的硫酸溶液和水,最后进行溶解;量筒与胶头滴管用于准确量取70%的硫酸溶液和水、烧杯用于完成溶解操作、玻璃棒用于溶解时的搅拌,故需要用到的是①②④⑤.
故选:B.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器是正确解答本题的关键.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案
相关题目
7.可用于除去氢氧化钠溶液中混有少量碳酸钠的试剂是( )
| A. | 氢氧化钡溶液 | B. | 盐酸 | C. | 氯化钡溶液 | D. | 硝酸银溶液 |
14.学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝是否也可作过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白.
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂.
【实验验证】
(1)把表格内容填写完整)①向试管内加适量的过氧化氢溶液;②Al2O3能作过氧化氢分解的催化剂
【得出结论】Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂.
(2)【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:
【实验目的】探究Al2O3在化学反应前后质量是否变化.
【实验步骤】①准确称量Al2O3(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤,洗涤,干燥,称量;④对比反应前后Al2O3的质量.
【交流讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂.
(3)【提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究Al2O3 在化学反应前后的化学性质是否改变.
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂.
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | ① | 有少量气泡 木条不复燃 | 常温下过氧化氢溶液分解速率很慢. |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 | 产生大量的气泡 木条复燃 | ② |
【得出结论】Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂.
(2)【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:
【实验目的】探究Al2O3在化学反应前后质量是否变化.
【实验步骤】①准确称量Al2O3(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤,洗涤,干燥,称量;④对比反应前后Al2O3的质量.
【交流讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂.
(3)【提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究Al2O3 在化学反应前后的化学性质是否改变.
8.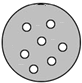 原子结构模型的建立经历了几代科学家的不断完善和修正,如图所示的结构模型为( )
原子结构模型的建立经历了几代科学家的不断完善和修正,如图所示的结构模型为( )
 原子结构模型的建立经历了几代科学家的不断完善和修正,如图所示的结构模型为( )
原子结构模型的建立经历了几代科学家的不断完善和修正,如图所示的结构模型为( )| A. | 道尔顿的实心球模型 | B. | 波尔的分层结构模型 | ||
| C. | 汤姆生的西瓜模型 | D. | 卢瑟福的核式结构模型 |
13.下列符号能表示一种元素,一个原子,还能表示一种物质的是( )
| A. | Cu | B. | H2 | C. | Cl | D. | O2 |