题目内容
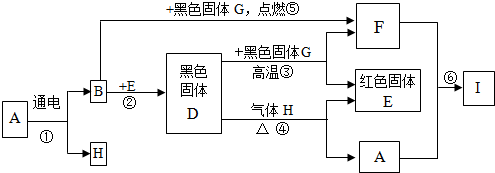
有一无色液体A,在通电条件下,可以产生B和H两种单质气体.其它关系如图所示,请完成下列问题.E是红色的金属单质.
(1)写出反应②的基本反应类型 .
(2)写出有关物质的化学式:A是 ,G是 ,I是 .
(3)请你说出H的一种用途: .

(1)写出反应②的基本反应类型
(2)写出有关物质的化学式:A是
(3)请你说出H的一种用途:
考点:物质的鉴别、推断,化学式的书写及意义,反应类型的判定
专题:框图型推断题
分析:此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,根据叙述的关键,以及物质的性质和物质之间的反应,做出判断,A通电能生成B和H,则A为水,B和H为“两种单质气体”,为氢气或氧气,黑色固体G能在B在这燃烧,则B为氧气,H为氢气,G可能为碳,F可能为二氧化碳;E为红色固体,则E为铜,与氧气反应生成的黑色固体D为氧化铜,代入框图,推断合理.
解答:解:根据图框和“有一无色液体A,在通电条件下,可以产生B和H两种单质气体”、“E是红色的金属单质”,则可推测:A通电能生成B和H,则A为水,B和H为“两种单质气体”,为氢气或氧气,黑色固体G能在B在这燃烧,则B为氧气,H为氢气,G可能为碳,F可能为二氧化碳;E为红色固体,则E为铜,与氧气反应生成的黑色固体D为氧化铜,代入框图,推断合理.
(1)B和E反应生成D,则此反应为两种物质生成一种物质的化合反应,所以本题答案为:化合反应;
(2)A通电能生成B和H,则A为水,B和H为氢气或氧气,黑色固体G能在B在这燃烧,则B为氧气,H为氢气,G可能为碳,F可能为二氧化碳,E为红色固体,则E为铜,与氧气反应生成的黑色固体D为氧化铜;I是二氧化碳与水反应生成碳酸,所以本题答案为:H2O,C;H2CO3
(3)H为氢气,其密度小,可填充气球;具有还原性,可冶炼金属;具有可燃性,生成物为水,可用作清洁能源(或制氨气等)等.
故答案为:
(1)化合反应;(2)H2O,C,H2CO3;(3)用作清洁能源(或制氨气等)
(1)B和E反应生成D,则此反应为两种物质生成一种物质的化合反应,所以本题答案为:化合反应;
(2)A通电能生成B和H,则A为水,B和H为氢气或氧气,黑色固体G能在B在这燃烧,则B为氧气,H为氢气,G可能为碳,F可能为二氧化碳,E为红色固体,则E为铜,与氧气反应生成的黑色固体D为氧化铜;I是二氧化碳与水反应生成碳酸,所以本题答案为:H2O,C;H2CO3
(3)H为氢气,其密度小,可填充气球;具有还原性,可冶炼金属;具有可燃性,生成物为水,可用作清洁能源(或制氨气等)等.
故答案为:
(1)化合反应;(2)H2O,C,H2CO3;(3)用作清洁能源(或制氨气等)
点评:本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.

练习册系列答案
相关题目
下列物质中不能与水形成溶液的是( )
| A、白糖 | B、食盐 |
| C、氢氧化钠 | D、植物油 |