题目内容
9. 水是人类宝贵的自然资源.
水是人类宝贵的自然资源.(1)天然水中含有许多杂质,实验室中常用过滤方法除去水中不溶性杂质,过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和玻璃棒(填仪器名称)
(2)硬水给生活和生产带来很多麻烦、生活中常用煮沸的方法降低水的硬度.
(3)氯气可用作自来水的消毒剂,实验室制取氯气的化学方程式为MnO2+4HCl(浓) $\frac{\underline{\;加热\;}}{\;}$MnCl2+Cl2↑+2H2O,MnO2不是(填“是”或“不是”)反应中的催化剂.
(4)甲和乙两种固体物质到溶解度曲线如图所示.
①t1℃时,甲和乙的溶解度相等(填“相等”或“不相等”).
②t2℃时,取甲和乙的饱和溶液各100g,两种溶液中溶剂的质量大小关系为甲<(填“>”“<”或“=”)乙.
③将t2℃时150g甲的饱和溶液降温至t1℃,所得溶液中溶质的质量分数为23.1%.
分析 (1)根据过滤过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和玻璃棒进行分析;
(2)根据生活中常用煮沸的方法降低水的硬度进行分析;
(3)根据催化剂在化学反应前后的质量和化学性质都没有变化进行分析;
(4)根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)过滤过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和玻璃棒;
(2)生活中常用煮沸的方法降低水的硬度;
(3)催化剂在化学反应前后的质量和化学性质都没有变化,但是该反应中二氧化锰反应后生成了氯化锰,所以二氧化锰不是该反应的催化剂;
(4)①通过分析溶解度曲线可知,t1℃时,甲和乙的溶解度相等;
②t2℃时,甲物质的溶解度大于乙物质的溶解度,所以取甲和乙的饱和溶液各100g,两种溶液中溶剂的质量大小关系为甲<乙;
③t2℃时甲物质的溶解度是50g,所以150g饱和溶液中含有甲50g,溶剂100g,t1℃时,甲物质的溶解度是30g,所以将t2℃时150g甲的饱和溶液降温至t1℃,所得溶液中溶质的质量分数为$\frac{30g}{130g}$×100%=23.1%.
故答案为:(1)玻璃棒;
(2)煮沸;
(3)不是;
(4)①相等;
②<;
③23.1%.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
20.铜、铁是人类使用最早、应用广泛的金属.
(一)对古代制品的认识
青铜铸件、丝绸织品、陶瓷器皿是我国古代劳动人民创造的辉煌成就.
1、上述制品不涉及到的材料是C(选填序号).
A、金属材料 B、无机非金属材料 C、复合材料
(2)如图1为出土文物古代青铜铸件“马踏飞燕”.该文物能保存至今的原因可能是AC(选填序号).
A、铜的活泼性弱 B、铜不会生锈 C、深埋于地下,隔绝空气
(二)铁、铜的冶炼
1、我国古代曾用孔雀石炼铜,涉及主要反应的化学方程式:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑+2CuO,2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
2、铁、铜矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2)、黄铜矿(CuFeS2)等.CuFeS2为二硫化亚铁铜,其中S元素的化合价为-2.
(1)工业炼铁大多采用赤铁矿、磁铁矿.以磁铁矿为原料炼铁反应的化学方程式为Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.炼铁不采用黄铁矿、黄铜矿,可能的原因是:
①黄铁矿、黄铜矿含铁量相对低;②冶炼过程中会产生有毒气体二氧化硫,污染环境.
(2)以黄铜矿为原料,采用生物炼铜是现代炼铜的新工艺,原理为:4CuFeS2+17O2+2H2SO4$\frac{\underline{\;耐酸、铜细菌\;}}{\;}$4CuSO4+2Fe2(SO4)3+2H2O.
向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu.
①发生主要反应的化学方程式:Fe+Fe2(SO4)3=3FeSO4,Fe+CuSO4=Cu+FeSO4.
②FeSO4溶液经蒸发浓缩、降温结晶、过滤等操作得到FeSO4•7H2O晶体.
(三)黄铜矿中铁、铜含量的测定
在科研人员指导下,兴趣小组称取25.00g黄铜矿(含少量Fe2O3和其它不含金属元素的杂质)模拟生物炼铜,使其全部转化为CuSO4、Fe2(SO4)3溶液.向溶液中加入过量NaOH溶液得到Cu(OH)2、Fe(OH)3固体.
1、证明NaOH溶液过量的方法:静置,向上层清液中滴加NaOH溶液,无现象.
2、用图2装置对固体进行热分解实验.
【资料】
①在68℃时,Cu(OH)2分解为CuO;在500℃时,Fe(OH)3分解为Fe2O3.
②在1400℃时,CuO分解为Cu2O和O2,Fe2O3分解为复杂的铁的氧化物和O2.
(1)装配好实验装置后,先要检查装置的气密性.
(2)停止加热后仍需继续通N2,可防止倒吸和使生成的气体全部被B和C装置吸收.
(3)控制不同的温度对A中固体加热,测得装置B和C中铜网的质量变化如表.
①此黄铜矿中铜、铁元素的质量分数:ω(Cu)%=25.60%;ω(Fe)%=26.88%.
②复杂的铁的氧化物化学式为Fe4O5.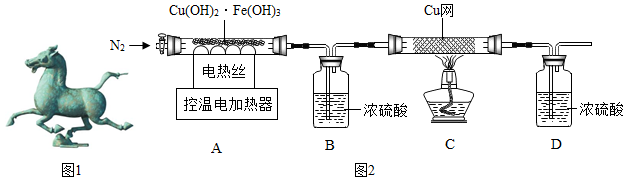
(一)对古代制品的认识
青铜铸件、丝绸织品、陶瓷器皿是我国古代劳动人民创造的辉煌成就.
1、上述制品不涉及到的材料是C(选填序号).
A、金属材料 B、无机非金属材料 C、复合材料
(2)如图1为出土文物古代青铜铸件“马踏飞燕”.该文物能保存至今的原因可能是AC(选填序号).
A、铜的活泼性弱 B、铜不会生锈 C、深埋于地下,隔绝空气
(二)铁、铜的冶炼
1、我国古代曾用孔雀石炼铜,涉及主要反应的化学方程式:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑+2CuO,2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
2、铁、铜矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2)、黄铜矿(CuFeS2)等.CuFeS2为二硫化亚铁铜,其中S元素的化合价为-2.
(1)工业炼铁大多采用赤铁矿、磁铁矿.以磁铁矿为原料炼铁反应的化学方程式为Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.炼铁不采用黄铁矿、黄铜矿,可能的原因是:
①黄铁矿、黄铜矿含铁量相对低;②冶炼过程中会产生有毒气体二氧化硫,污染环境.
(2)以黄铜矿为原料,采用生物炼铜是现代炼铜的新工艺,原理为:4CuFeS2+17O2+2H2SO4$\frac{\underline{\;耐酸、铜细菌\;}}{\;}$4CuSO4+2Fe2(SO4)3+2H2O.
向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu.
①发生主要反应的化学方程式:Fe+Fe2(SO4)3=3FeSO4,Fe+CuSO4=Cu+FeSO4.
②FeSO4溶液经蒸发浓缩、降温结晶、过滤等操作得到FeSO4•7H2O晶体.
(三)黄铜矿中铁、铜含量的测定
在科研人员指导下,兴趣小组称取25.00g黄铜矿(含少量Fe2O3和其它不含金属元素的杂质)模拟生物炼铜,使其全部转化为CuSO4、Fe2(SO4)3溶液.向溶液中加入过量NaOH溶液得到Cu(OH)2、Fe(OH)3固体.
1、证明NaOH溶液过量的方法:静置,向上层清液中滴加NaOH溶液,无现象.
2、用图2装置对固体进行热分解实验.
【资料】
①在68℃时,Cu(OH)2分解为CuO;在500℃时,Fe(OH)3分解为Fe2O3.
②在1400℃时,CuO分解为Cu2O和O2,Fe2O3分解为复杂的铁的氧化物和O2.
(1)装配好实验装置后,先要检查装置的气密性.
(2)停止加热后仍需继续通N2,可防止倒吸和使生成的气体全部被B和C装置吸收.
(3)控制不同的温度对A中固体加热,测得装置B和C中铜网的质量变化如表.
| 温度/℃ | 室温 | 100 | 550 | 1400 |
| B装置/g | 200.00 | 201.80 | 205.04 | 205.04 |
| C中铜网/g | 100.00 | 100.00 | 100.00 | 101.28 |
②复杂的铁的氧化物化学式为Fe4O5.

17.下列反映其对应关系的图象中错误的是( )
| A. |  向一定量稀硫酸和硫酸钠的混合溶液中不断加入氢氧化钡溶液 | |
| B. |  向一定量的氢氧化钡溶液中不断加入稀硫酸 | |
| C. |  向分别盛有相同质量镁和铁的试管中,分别加入等溶质质量分数的稀盐酸至过量 | |
| D. |  将相同质量的粉状碳酸钙和块状碳酸钙与足量相同溶质质量分数的稀盐酸混合 |
4.下列变化中属于化学变化的是( )
| A. | 河水结冰 | B. | 汽油挥发 | C. | 葡萄酿酒 | D. | 干冰升华 |
1.下列各组离子在溶液中能大量共存的是( )
| A. | H+、Cl-、OH-、Na+ | B. | H+、Ca2+、SO42-、HCO3- | ||
| C. | Ba2-、H+、Cl-、SO42- | D. | Cu2+、Na+、Cl-、SO42- |
19.对与化学反应X+Na2CO3═2Y+CaCO3↓的分析过程的是( )
| A. | 该反应属于复分解反应 | B. | Y中一定含有钠元素 | ||
| C. | X一定是熟石灰 | D. | X中阴离子化合价是-1价 |

 根据下图中的粒子结构示意图,回答下列问题:
根据下图中的粒子结构示意图,回答下列问题: