��Ŀ����
����������Һ�ڴ�Ź����л���Ȼ�ֽ⣬ʹ��������������С��ijͬѧʹ��һƿԭ��עΪ30%�Ĺ���������Һ�����ȡ������ʵ�飮ͨ����������ƿ�й���116.8g��Һ��ȡ��13.6g��һ�������½���ʵ�飬������������������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ���Լ���
��1��������ƿ����������Һ����������������
��2����ƿ��Һ�У��Ѿ��ֽ�Ĺ�������������

���𰸡�
25%��6.8g
��������
�����������ͼ���Կ��������ɵ�����������Ϊ1.6g������Ҫ�������������Ϊx
2H2O2 2H2O+O2��
2H2O+O2��
68 32
x 1.6g
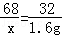 x=3.4g
x=3.4g
����Һ��������������Ϊ��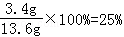 ��
��
��2�����ѷֽ�Ĺ������������Ϊy�����ɵ�����������Ϊz
2H2O2 2H2O+O2��
2H2O+O2��
68 32
y z
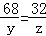 z=
z=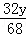
��116.8g+z����30%=116.8g��25%+y
y=6.8g
��������ƿ����������Һ����������������25%����ƿ��Һ�У��Ѿ��ֽ�Ĺ�������������6.8g��
���㣺���ݻ�ѧ��Ӧ����ʽ�ļ��㣻�й��������������ļ��㣮

��ϰ��ϵ�д�
�����Ŀ
 ����������Һ�ڴ�Ź����лỺ���ֽ⣮��ͼΪʵ���ұ����һƿ����������Һ�ı�ǩ��ijС��ͬѧΪ�˽��������ķֽ������ȡ5g����Һ���Ƶ�0.64g�������Է�������
����������Һ�ڴ�Ź����лỺ���ֽ⣮��ͼΪʵ���ұ����һƿ����������Һ�ı�ǩ��ijС��ͬѧΪ�˽��������ķֽ������ȡ5g����Һ���Ƶ�0.64g�������Է�������
 ��2013?��̨��һģ������������Һ�ڴ�Ź����л���Ȼ�ֽ⣬ʹ��������������С��ijͬѧʹ��һƿԭ��עΪ30%�Ĺ���������Һ�����ȡ������ʵ�飮ͨ����������ƿ�й���116.8g��Һ��ȡ��13.6g��һ�������½���ʵ�飬������������������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ���Լ���
��2013?��̨��һģ������������Һ�ڴ�Ź����л���Ȼ�ֽ⣬ʹ��������������С��ijͬѧʹ��һƿԭ��עΪ30%�Ĺ���������Һ�����ȡ������ʵ�飮ͨ����������ƿ�й���116.8g��Һ��ȡ��13.6g��һ�������½���ʵ�飬������������������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ���Լ��� ����������Һ�ڴ�Ź����лỺ���ֽ⣮��ͼ��ʵ���ұ����һƿ����������Һ��ijС��16ѧΪ�˽��������ķֽ������ȡ10g����Һ���Ƶ�1.28g�������Է���������ƿ����������Һ�ڱ���������Ѿ��ֽ�Ĺ��������������
����������Һ�ڴ�Ź����лỺ���ֽ⣮��ͼ��ʵ���ұ����һƿ����������Һ��ijС��16ѧΪ�˽��������ķֽ������ȡ10g����Һ���Ƶ�1.28g�������Է���������ƿ����������Һ�ڱ���������Ѿ��ֽ�Ĺ�������������� ����������Һ�ڴ�Ź����лỺ���ֽ⣮��ͼΪijУʵ���ұ����һƿ����������Һ�ı�ǩ��ijС��ͬѧΪ�˽��������ķֽ����������ƿ��Һȫ��������ȡ����������乲�ų�����32g��������ˮ�ֵ�����������ʣ����Һ����������������
����������Һ�ڴ�Ź����лỺ���ֽ⣮��ͼΪijУʵ���ұ����һƿ����������Һ�ı�ǩ��ijС��ͬѧΪ�˽��������ķֽ����������ƿ��Һȫ��������ȡ����������乲�ų�����32g��������ˮ�ֵ�����������ʣ����Һ����������������