题目内容
7. 如图,在盛有少量石灰石的试管中加入适量的稀盐酸,回答下列问题:
如图,在盛有少量石灰石的试管中加入适量的稀盐酸,回答下列问题:(1)试管中观察到的现象有石灰石逐渐减少,固体表面有气泡产生
(2)铁架台在实验中的一般作用是固定和支持各种仪器,一般常用于过滤、加热等实验操作;
(3)此实验中澄清石灰水的作用是检验是否有二氧化碳产生
(4)烧杯中导管口冒气泡是由于反应,装置内气体增多,气压增大,大于外界大气压,在压强差的作用下,导管口产生气泡.
分析 根据石灰石与稀盐酸反应生成氯化钙、水和二氧化碳,结合二氧化碳能使澄清的石灰水变浑浊,进行分析解答.
解答 解:
(1)石灰石和稀盐酸反应生成二氧化碳气体,所以石灰石逐渐减少,固体表面有气泡产生;
(2)铁架台在实验中用于固定和支持各种仪器,一般常用于过滤、加热等实验操作
(3)二氧化碳能使澄清石灰水变浑浊,澄清石灰水的作用是检验是否有二氧化碳产生;
(4)石灰石和稀盐酸反应生成二氧化碳气体,导致管中的气体增多,导致内部压强变大,装置内部压强大于外界大气压,在压强差的作用下气体从导管口被压出,因此在试管中观察到的实验现象是有大量气泡产生;
故答案为:(1)石灰石逐渐减少,固体表面有气泡产生
(2)固定和支持各种仪器,一般常用于过滤、加热等实验操作
(3)检验是否有二氧化碳产生 (4)增多,气压增大,大于外界大气压
点评 本题难度不大,掌握二氧化碳的化学性质是正确解答本题的关键.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
7.某学生测定下列数据合理的是( )
| A. | 用100ml量筒量取7.5ml水 | |
| B. | 用10ml量筒量取8.5ml水 | |
| C. | 用托盘天平称得某食盐样品的质量为15.56g | |
| D. | 用烧杯量取200.0ml的盐酸 |
8.石灰厂为了测定一批石灰石样品中碳酸钙的质量分数.取用8g石灰石样品.把24g稀盐酸分4次加人样品中(样品中除碳酸钙外.杂质既不与盐酸反应.也不溶于水).充分反应后经过滤.干燥等操作.最后称量.得实验数据如表:
试回答下列问题:
(1)该石灰石样品中碳酸钙的质量分数是62.5%.
(2)生成的二氧化碳气体多少克?
| 稀盐酸的用量 | 第一次加入6g | 第二次加入6g | 第三次加入6g | 第四次加入6g |
| 剩余固体的质量 | 6g | 4g | 3g | 3g |
(1)该石灰石样品中碳酸钙的质量分数是62.5%.
(2)生成的二氧化碳气体多少克?
2.下列物质的应用正确的是( )
| A. |  氧气作燃料炼钢 | B. |  氩气用于飞艇 | ||
| C. |  液氮冷冻机 | D. |  用稀有气体填充闪光灯 |
16.资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学设计了如下实验方案,验证反应产物并探究发生反应的化学方程式.
已知:①MgCO3和Mg(OH)2均为白色不溶物.
②MgCO3和Mg(OH)2均可跟盐酸发生复分解反应.
③酚酞遇碳酸氢钠溶液呈浅红色,酚酞遇碳酸钠溶液呈红色.
④CaCl2+Na2CO3═CaCO3↓+2NaCl
(1)提出假设
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红.
该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能是MgCO3
猜测2:白色不溶物可能是Mg(OH)2
猜测3:白色不溶物可能是MgCO3和Mg(OH)2的混合物.
(2)设计定性实验确定产物并验证猜测:
(3)为进一步确定实验I的产物,设计定量实验方案,如图所示:
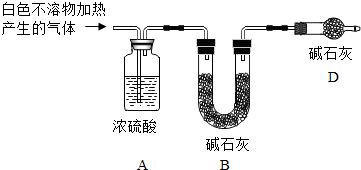
已知:MgCO3$\frac{\underline{\;\;△\;\;}}{\;}$MgO+CO2↑
Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O
碱石灰可以吸收二氧化碳和水蒸气
①右图所示实验装置D中碱石灰的作用是防止空气中的二氧化碳和水蒸气被B中碱石灰吸收,造成实验误差.
②称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中.实验前后装置A增重1.8g,装置B增重8.8g,请分析数据并结合实验Ⅱ、Ⅲ、Ⅳ的结论,补全镁与饱和碳酸氢钠溶液反应的化学方程式:3MgMg+4NaHCO3+2H2O═2MgCO3↓+Mg(OH)2↓+3H2↑+2Na2CO3.
已知:①MgCO3和Mg(OH)2均为白色不溶物.
②MgCO3和Mg(OH)2均可跟盐酸发生复分解反应.
③酚酞遇碳酸氢钠溶液呈浅红色,酚酞遇碳酸钠溶液呈红色.
④CaCl2+Na2CO3═CaCO3↓+2NaCl
(1)提出假设
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红.
该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能是MgCO3
猜测2:白色不溶物可能是Mg(OH)2
猜测3:白色不溶物可能是MgCO3和Mg(OH)2的混合物.
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验操作 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验I中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体为氢气 |
| 实验Ⅲ | ①取实验I中少量的白色悬浊液,过滤,洗涤干净沉淀, 之后向沉淀中加入足量稀盐酸 | ②产生气泡,沉淀全部溶解 | 白色不溶物含有MgCO3 |
| 实验Ⅳ | 取实验I中的澄清液,向其中加入少量CaCl2稀溶液 | 只有白色沉淀产生 | ③澄清液中一定含有的溶质是Na2CO3(填化学式) |

已知:MgCO3$\frac{\underline{\;\;△\;\;}}{\;}$MgO+CO2↑
Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O
碱石灰可以吸收二氧化碳和水蒸气
①右图所示实验装置D中碱石灰的作用是防止空气中的二氧化碳和水蒸气被B中碱石灰吸收,造成实验误差.
②称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中.实验前后装置A增重1.8g,装置B增重8.8g,请分析数据并结合实验Ⅱ、Ⅲ、Ⅳ的结论,补全镁与饱和碳酸氢钠溶液反应的化学方程式:3MgMg+4NaHCO3+2H2O═2MgCO3↓+Mg(OH)2↓+3H2↑+2Na2CO3.