题目内容
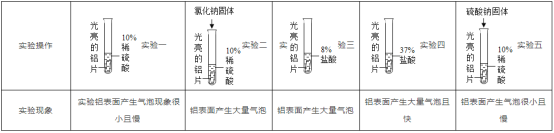
有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成。为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性,经过思考设计并进行了以下实验:

(1)白色粉末中一定不含_____________;可能含有____________。
(2)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。
(提出问题)无色滤液中呈碱性的物质是什么?
(作出猜想)猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
① 取无色滤液少许于试管中,滴加过量的BaCl2溶液 | ________ | 猜想Ⅱ不成立 |
② 在①反应后的试管中滴加________ | 溶液变为红色 | 猜想Ⅲ成立 |
(得出结论)白色粉末的成分是________________。
练习册系列答案
相关题目
为测定某样品(碳酸钠和氯化钠的混合物)中碳酸钠的质量分数,某化学兴趣小组进行以下实验,取50g的样品放置于气体发生装置中,然后取一定溶质质量分数的稀盐酸分5次加到该气体发生装置中,每次向装样品的烧杯中加入25g,实验测得加入稀盐酸的质量与实验时所得气体的质量的关系如下表。求:
加入稀盐酸的质量/g | 25 | 50 | 75 | 100 | 125 |
所得气体的质量/g | 4.4 | m | 4.4 | 4.4 | 0 |
(1)表中m的值为________。
(2)样品中碳酸钠的质量分数是________(精确到0.1%)。
(3)所用稀盐酸的溶质质量分数________(写出具体的计算过程)。


 液体读数 B.
液体读数 B.  滴加液体
滴加液体 加热固体 D.
加热固体 D. 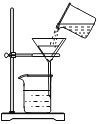 过滤操作
过滤操作