题目内容
除去食盐水中的CaCl2和Na2SO4杂质的操作有:①加过量的BaCl2溶液;②过滤;③加过量的Na2CO3溶液;④蒸发结晶;⑤加适量盐酸。下列操作顺序正确的是(提示BaSO4、BaCO3难溶于水)
A. ③①②⑤④ B. ①⑤③②④ C. ①③⑤④② D. ①③②⑤④
水和溶液在生产、生活中起着十分重要的作用,请回答下列问题。
(1)请完成鉴别硬水和软水的实验报告。
实验步骤 | 实验现象及结论 |
___ | ___ |
(2)电解水实验装置如图甲所示,a管产生的气体是___,用燃着的木条靠近该管尖嘴处,打开活塞,可观察到的现象___。

(3)图乙是氢氧化钙的溶解度曲线。40℃时,氢氧化钙的溶解度是0.14g,这句话的含义是___。将室温下的饱和氢氧化钙溶液升温(不超过100℃),发现氢氧化钙溶液变浑浊,请根据溶解度曲线解释原理:___。
(4)某石灰水含有氢氧化钙1.48g,要使该石灰水中的氢氧化钙全部转化为碳酸钙沉淀,至少需要二氧化碳的质量是_____?(请在答题纸上写出完整的解题过程)
有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成。为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性,经过思考设计并进行了以下实验:
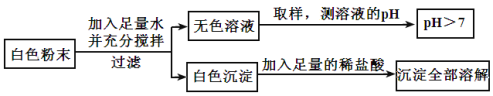
(1)白色粉末中一定不含_____________;可能含有____________。
(2)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。
(提出问题)无色滤液中呈碱性的物质是什么?
(作出猜想)猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
① 取无色滤液少许于试管中,滴加过量的BaCl2溶液 | ________ | 猜想Ⅱ不成立 |
② 在①反应后的试管中滴加________ | 溶液变为红色 | 猜想Ⅲ成立 |
(得出结论)白色粉末的成分是________________。
除去下列物质中的少量杂质,所用试剂及方法不正确的是( )
选项 | 物质 | 杂质 | 试剂及方法 |
A | NaCl固体 | 泥沙 | 加水溶液、过滤、蒸发 |
B | KNO3溶液 | Ba(OH)2 | 滴加适量K2SO4溶液、过滤 |
C | Na2SO4溶液 | Na2CO3 | 滴加稀盐酸至不在产生气泡 |
D | N2 | O2 | 通过红热的铜网 |
A. A B. B C. C D. D


