题目内容
将3.6 g碳酸钙高温煅烧一段时间后冷却,测得固体剩余物中钙元素的质量分数为57.6%,求固体剩余物中氧化钙的质量.
解析:
| 根据质量守恒定律,参加化学反应前后各元素的种类、质量不变,可知钙元素的质量相等,且CaCO3中Ca元素质量分数为40%.
设剩余固体质量为x,剩余物中氧化钙的质量为y. 3.6 g×40%=x×57.6% x=2.5 g 根据质量守恒定律 3.6 g-2.5 g=1.1 g 56∶44=y∶1.1 g y=1.4 g 答案:剩余物中的氧化钙的质量为1.4 g
|
提示:

 阅读快车系列答案
阅读快车系列答案某校化学兴趣小组的同学学习了酸、碱、盐的知识后,对课本中“酸、碱、盐之间并不是都能发生复分解反应”这句话产生了兴趣,展开了探究性学习.
(1)【提出问题】发生复分解反应应具备哪些条件?
(2)【活动探究】该小组同学进行以下四组实验,发现均能反应,写出反应④的化学方程式:
①硝酸钡溶液与稀硫酸 ②稀硫酸与碳酸钾溶液 ③稀盐酸与氢氧化钠溶液 ④硝酸钡溶液与碳酸钾溶液:______.
(3)【理论分析】上述反应未什么能够发生?是因为在这些反应物的溶液中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水.如:
①中有Ba2++SO42-→BaSO4↓ ②中有H++CO32-→H2O+CO2↑ ③中有H++OH-→H2O ④中有______两种离子,所以才发生化学反应.
(4)【得出结论】经过分析,该小组同学得出以下结论:生成物中是否有沉淀或气体或水,是判断酸、碱、盐之间能否发生复分解反应的主要条件.
(5)【形成网络】按照一定的顺序排列某些离子,就可以形成一种知识网络.在网络中,用“--”相连接的阴、阳离子间能两两结合生成沉淀或气体或水.现有Ca2+、HCO3-两种离子,请将它们填入下面合适的“ ”内,使其形成一个更为完整的复分解反应的知识网络.
”内,使其形成一个更为完整的复分解反应的知识网络.

(6)【拓展应用】根据得出的结论,解决以下问题:
已知t℃时四种化合物在溶剂A和溶剂B中各自的溶解度(g/100g溶剂)如下表所示.
| 物质 | 在溶剂A中的溶解度 | 在溶剂B中的溶解度 |
| AgNO3 | 170 | 86 |
| Ba(NO3)2 | 9.3 | 97.2 |
| AgCl | 1.5×10-4 | 0.8 |
| BaCl2 | 33.3 | 约为0 |
则表中四种化合物中某两种化合物在溶剂B中能发生复分解反应的化学方程式为:______.
溶液的应用非常广泛K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下:
| 温度/℃ | 20 | 30 | 50 | 60 | 80 |
|
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 |

(1)图1中能表示KNO3溶解曲线的是 (填“甲”或“乙”)
(2)曲线上M点的含义是 .
(3)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.下列有关说法中,正确的有 .
A.烧杯①中溶解的是KNO3,烧杯②中溶解的是K2CO3
B.烧杯②中溶液是不饱和溶液
C.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数一定减小
D.将得到的烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能不变.
溶液的应用非常广泛.K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下:
| 温度/℃ | 20 | 30 | 50 | 60 | 80 |
|
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 |
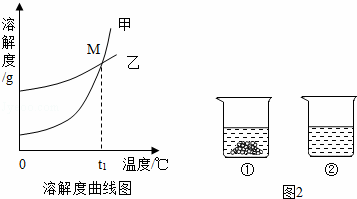
(1)硝酸钾溶液中的溶剂是 .
(2)图中能表示KNO3溶解度曲线的是 (填“甲”或“乙”).
(3)溶解度曲线上M点的含义是 .
(4)现有200g溶质质量分数为10%的碳酸钾溶液,若使溶液的溶质质量分数增加一倍,应该蒸发掉 g水.
(5)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.下列有关说法中,正确的是 D (填字母序号).
A.烧杯②中溶液一定是不饱和溶液
B.若使烧杯①中固体全部溶解,溶液中溶质质量分数一定增大
C.将烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能增大
D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数可能增大.
溶液的应用非常广泛.K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下:
| 温度/℃ | 20 | 30 | 50 | 60 | 80 |
|
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 |

(1)硝酸钾溶液中的溶剂是 .
(2)图中能表示KNO3溶解度曲线的是 (填“甲”或“乙”).
(3)溶解度曲线上M点的含义是 .
(4)现有200g溶质质量分数为10%的碳酸钾溶液,若使溶液的溶质质量分数增加一倍,应该蒸发掉 g水.
(5)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.下列有关说法中,正确的是 D (填字母序号).
A.烧杯②中溶液一定是不饱和溶液
B.若使烧杯①中固体全部溶解,溶液中溶质质量分数一定增大
C.将烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能增大
D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数可能增大.