题目内容
用含杂质(杂质不溶于水,也不与酸反应)的铁10g与50g稀硫酸充分反应,铁消耗完,滤去杂质,溶液的质量为58.1g.则此铁的纯度是( )A.28%
B.56%
C.84%
D.无法确定
【答案】分析:通过假设铁的质量,根据反应中铁与产生氢气的质量关系,利用质量守恒定律,解决所假设的铁的质量即可完成此铁的纯度的计算.
解答:解:(方法一)设铁的质量为x,结合Fe+H2SO4═FeSO4+H2↑
56 2
可以知道完全反应生成氢气的质量=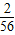 x,
x,
根据质量守恒定律,x+50g=58.1g+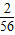 x,解得x=8.4g
x,解得x=8.4g
则此铁的纯度=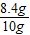 ×100%=56%.
×100%=56%.
(方法二)设铁的质量为x
Fe+H2SO4═FeSO4+H2↑ 溶液增加的质量
56 98 152 54
x 58.1g-50g=8.1g
 =
=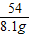
解得:x=8.4g
则此铁的纯度=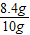 ×100%=56%.
×100%=56%.
故选C.
点评:金属铁在与酸反应中呈现出+2价,利用一定量金属完全反应产生氢气质量=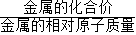 ×金属质量时,铁元素的化合价应使用+2价.
×金属质量时,铁元素的化合价应使用+2价.
解答:解:(方法一)设铁的质量为x,结合Fe+H2SO4═FeSO4+H2↑
56 2
可以知道完全反应生成氢气的质量=
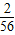 x,
x,根据质量守恒定律,x+50g=58.1g+
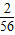 x,解得x=8.4g
x,解得x=8.4g则此铁的纯度=
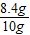 ×100%=56%.
×100%=56%.(方法二)设铁的质量为x
Fe+H2SO4═FeSO4+H2↑ 溶液增加的质量
56 98 152 54
x 58.1g-50g=8.1g
 =
=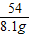
解得:x=8.4g
则此铁的纯度=
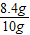 ×100%=56%.
×100%=56%.故选C.
点评:金属铁在与酸反应中呈现出+2价,利用一定量金属完全反应产生氢气质量=
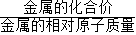 ×金属质量时,铁元素的化合价应使用+2价.
×金属质量时,铁元素的化合价应使用+2价. 
练习册系列答案
相关题目
目前,许多城市用PVC管更换了旧自来水铁质管道,基本解决了管内生锈、饮用水含铁量超标的问题.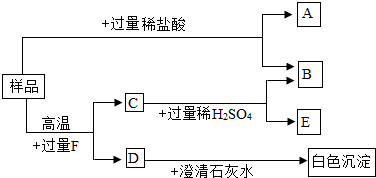
(1)PVC管属于 制品(填代号). ①金属 ②纤维 ③塑料 ④橡胶
(2)通常与铁质管道生锈有关的物质有 、 .防止铁制品生锈的一种方法是 .
(3)某课外小组截取一段旧铁质管道作样品,粉碎后按右图所示步骤进行实验.已知B是气体单质,F在常温下为气态化合物.
①溶液A中的溶质有 、 、 ;
②澄清石灰水与D反应的化学方程式为: ;
③样品与过量F反应的化学方程式为: .
(4)某化学兴趣小组的同学对一批未生锈的铁质管道样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中只有一位同学所用的稀硫酸与铁样品恰好完全反应.实验数据如表:
① 同学所用的稀硫酸与铁样品恰好完全反应;
②样品中的铁的质量分数是 ;
③计算恰好完全反应后所得溶液中溶质的质量分数.(烧杯质量为25.4克)

(1)PVC管属于
(2)通常与铁质管道生锈有关的物质有
(3)某课外小组截取一段旧铁质管道作样品,粉碎后按右图所示步骤进行实验.已知B是气体单质,F在常温下为气态化合物.
①溶液A中的溶质有
②澄清石灰水与D反应的化学方程式为:
③样品与过量F反应的化学方程式为:
(4)某化学兴趣小组的同学对一批未生锈的铁质管道样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中只有一位同学所用的稀硫酸与铁样品恰好完全反应.实验数据如表:
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸 | 200g | 150g | 150g |
| 加入的铁样品 | 9g | 9g | 14g |
| 充分反应后,烧杯+剩余物 | 208.7g | 158.7g | 163.7g |
②样品中的铁的质量分数是
③计算恰好完全反应后所得溶液中溶质的质量分数.(烧杯质量为25.4克)
目前,许多城市用PVC管更换了旧自来水铁质管道,基本解决了管内生锈、饮用水含铁量超标的问题.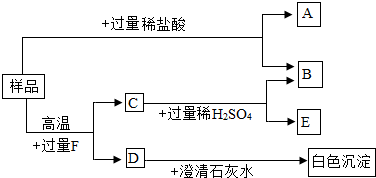
(1)PVC管属于______制品(填代号). ①金属 ②纤维 ③塑料 ④橡胶
(2)通常与铁质管道生锈有关的物质有______、______.防止铁制品生锈的一种方法是______.
(3)某课外小组截取一段旧铁质管道作样品,粉碎后按右图所示步骤进行实验.已知B是气体单质,F在常温下为气态化合物.
①溶液A中的溶质有______、______、______;
②澄清石灰水与D反应的化学方程式为:______;
③样品与过量F反应的化学方程式为:______.
(4)某化学兴趣小组的同学对一批未生锈的铁质管道样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中只有一位同学所用的稀硫酸与铁样品恰好完全反应.实验数据如表:
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸 | 200g | 150g | 150g |
| 加入的铁样品 | 9g | 9g | 14g |
| 充分反应后,烧杯+剩余物 | 208.7g | 158.7g | 163.7g |
②样品中的铁的质量分数是______;
③计算恰好完全反应后所得溶液中溶质的质量分数.(烧杯质量为25.4克)