题目内容
将氢氧化钠固体投入到200.0g一定溶质质量分数的稀硫酸中,恰好完全反应,所得溶液的质量为208.0g.请计算所用稀硫酸的溶质质量分数.
【答案】分析:根据质量守恒定律可知,参加反应的氢氧化钠的质量为208.0g-200g=80g,根据氢氧化钠与硫酸反应的方程式,由氢氧化钠的质量可求出稀硫酸溶液中溶质的质量,再根据溶质质量分数的计算公式计算即可.
解答:解:由质量守恒定律可知,参加反应的氢氧化钠的质量为208.0g-200g=8g
设稀硫酸中溶质的质量x
H2SO4 +2NaOH=2H2O+Na2SO4
98 80
x 8g
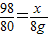 解得:x=9.8g
解得:x=9.8g
所用稀硫酸的溶质质量分数为: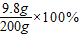 =4.9%
=4.9%
答:所用稀硫酸的溶质质量分数为4.9%.
点评:本题主要考查学生运用化学方程式进行计算的能力,掌握相关的溶液及化学方程式基本计算是解题的关键所在.
解答:解:由质量守恒定律可知,参加反应的氢氧化钠的质量为208.0g-200g=8g
设稀硫酸中溶质的质量x
H2SO4 +2NaOH=2H2O+Na2SO4
98 80
x 8g
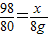 解得:x=9.8g
解得:x=9.8g所用稀硫酸的溶质质量分数为:
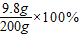 =4.9%
=4.9%答:所用稀硫酸的溶质质量分数为4.9%.
点评:本题主要考查学生运用化学方程式进行计算的能力,掌握相关的溶液及化学方程式基本计算是解题的关键所在.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
 20、通过“金属和金属材料”和“燃烧”的复习,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:
20、通过“金属和金属材料”和“燃烧”的复习,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题: 为了探究空气中所含氧气的体积,某同学设计了如下实验方案:将一个50mL的空量筒倒扣在水中,量筒内外的液面均位于量筒的40mL刻度处.量筒内浮着一个铜制的小船,船中放有少量白磷,如图所示.
为了探究空气中所含氧气的体积,某同学设计了如下实验方案:将一个50mL的空量筒倒扣在水中,量筒内外的液面均位于量筒的40mL刻度处.量筒内浮着一个铜制的小船,船中放有少量白磷,如图所示.