题目内容
学校运动会上短跑项目“发令枪”里的火药成分为KClO3,MnO2和红磷,当扣动扳机时,①撞针撞击火药,产生热量使KClO3分解产生O2②并引燃红磷产生白烟.试分别写这两步反应的化学方程式.
① ;
② 基本反应类型是 .
(2)“84”消毒液可用于灾区防疫,其主要成分是次氯酸钠(NaClO),制取它的化学方程式为2NaOH+X═NaClO+NaCl+H2O,则X的化学式为 .求出NaClO中氯元素化合价并在该化学式中表示出来.
(3)固体MgH2是氢能源汽车的供能剂,MgH2可以和水反应生成一种碱,同时释放出氢气,该反应的化学方程式是 .
答案 分析:
(1)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写并分析反应的类型;
(2)根据质量守恒定律来书写化学式并计算化合物中元素的化合价;
(3)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解:(1)①氯酸钾受热分解为氯化钾和氧气,化学方程式为:2KClO3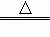 2KCl+3O2↑;
2KCl+3O2↑;
②磷和氧气在点燃的条件下反应生成五氧化二磷,反应是两种,生成物是一种,符合化合反应的概念,化学方程式为:4P+5O2 2P2O5;
2P2O5;
(2)化学反应前后原子种类和个数不变,反应后有两个钠原子、两个氢原子、两个氧原子、两个氯原子,反应前有两个钠原子、两个氧原子和两个氢原子,故一个X分子中含有两个氯原子,化学式为Cl2;
在NaClO中,Na元素的化合价为+1价,O元素的化合价为﹣2价,
设次氯酸钠中氯元素的化合价为x,
根据化合物中元素的正负化合价的代数和为0,则
+1+x+(﹣2)=0
解得x=+1;化合价要标注在元素符号的正上方;
(3)根据题意知反应物为MgH2和水,生成为碱和氢气,碱应该是氢氧化镁,配平后得MgH2+2H2O=Mg(OH)2↓+2H2↑.
故答案为:(1)①2KClO3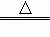 2KCl+3O2↑;
2KCl+3O2↑;
②4P+5O2 2P2O5;化合反应;
2P2O5;化合反应;
(2)Cl2;Na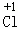 O;
O;
(3)MgH2+2H2O=Mg(OH)2+2H2↑.


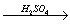 H2
H2  Cu; (2)CuO
Cu; (2)CuO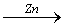 Cu
Cu