题目内容
请用所学的化学知识解释下列现象:
(1)NaOH在生活中可用来除去油污,是因为氢氧化钠能与 反应;
(2)一氧化碳用于炼铁的原理(用化学方程式表示) ;
(3)用天然气作燃料的原理(用化学方程式表示) ;
(4)将一包放置较长时间的食品干燥剂放入烧杯中,放入足量的稀盐酸,可能发生反应的化学方程式是 、 、 .(写三个即可)
(1)NaOH在生活中可用来除去油污,是因为氢氧化钠能与
(2)一氧化碳用于炼铁的原理(用化学方程式表示)
(3)用天然气作燃料的原理(用化学方程式表示)
(4)将一包放置较长时间的食品干燥剂放入烧杯中,放入足量的稀盐酸,可能发生反应的化学方程式是
考点:常见碱的特性和用途,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律,常见的碱 碱的通性
分析:(1)根据氢氧化钠的碱性分析;
(2)用磁铁矿炼铁的反应原理是在高温条件下,利用焦炭与氧气反应生成的一氧化碳作还原剂,从铁矿石中将铁还原出来.
(3)天然气的主要成分是甲烷,甲烷燃烧生成二氧化碳和水,写出反应的化学方程式即可;
(4)生石灰与水反应生成氢氧化钙,可做食品干燥剂,一包放置较长时间的食品干燥剂中可能含有氧化钙、氢氧化钙和碳酸钙.
(2)用磁铁矿炼铁的反应原理是在高温条件下,利用焦炭与氧气反应生成的一氧化碳作还原剂,从铁矿石中将铁还原出来.
(3)天然气的主要成分是甲烷,甲烷燃烧生成二氧化碳和水,写出反应的化学方程式即可;
(4)生石灰与水反应生成氢氧化钙,可做食品干燥剂,一包放置较长时间的食品干燥剂中可能含有氧化钙、氢氧化钙和碳酸钙.
解答:解:(1)氢氧化钠具有碱性,可以与油脂发生反应,而除去油污;
(2)炼铁是将原料(铁矿石、焦炭、石灰石、空气)通入高炉中,在高炉中发生复杂反应,生成铁的单质,例如以赤铁矿为例,氧化铁和一氧化碳反应生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO
2Fe+3CO2.
(3)天然气的主要成分是甲烷,甲烷燃烧生成二氧化碳和水,反应的化学方程式为:CH4+2O2
CO2+2H2O
(4)首先生石灰与水反应生成氢氧化钙,方程式为CaO+H2O=Ca(OH)2.
生石灰与盐酸反应生成氯化钙和水,CaO+2HCl═CaCl2+H2O,
氢氧化钙与盐酸反应生成氯化钙和水,Ca(OH)2+2HCl═CaCl2+2H2O,
碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,CaCO3+2HCl═CaCl2+H2O+CO2↑.
故答案为:(1)油脂(2)Fe2O3+3CO
2Fe+3CO2(3)CH4+2O2
CO2+2H2O
(4)CaO+H2O=Ca(OH)2;CaO+2HCl═CaCl2+H2O;Ca(OH)2+2HCl═CaCl2+2H2O(或CaCO3+2HCl═CaCl2+H2O+CO2↑).
(2)炼铁是将原料(铁矿石、焦炭、石灰石、空气)通入高炉中,在高炉中发生复杂反应,生成铁的单质,例如以赤铁矿为例,氧化铁和一氧化碳反应生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO
| ||
(3)天然气的主要成分是甲烷,甲烷燃烧生成二氧化碳和水,反应的化学方程式为:CH4+2O2
| ||
(4)首先生石灰与水反应生成氢氧化钙,方程式为CaO+H2O=Ca(OH)2.
生石灰与盐酸反应生成氯化钙和水,CaO+2HCl═CaCl2+H2O,
氢氧化钙与盐酸反应生成氯化钙和水,Ca(OH)2+2HCl═CaCl2+2H2O,
碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,CaCO3+2HCl═CaCl2+H2O+CO2↑.
故答案为:(1)油脂(2)Fe2O3+3CO
| ||
| ||
(4)CaO+H2O=Ca(OH)2;CaO+2HCl═CaCl2+H2O;Ca(OH)2+2HCl═CaCl2+2H2O(或CaCO3+2HCl═CaCl2+H2O+CO2↑).
点评:本题主要考查物质的性质和用途及其化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
相关题目
下列各组物质投入水中,搅拌后能得到无色、澄清溶液的是( )
| A、KNO3、HCl、CuCl2 |
| B、Ca(OH)2、BaCl2、Na2SO4 |
| C、Na2CO3、NaCl、Ca(OH)2 |
| D、NaOH、KCl、H2SO4 |
金属钠非常活泼,能与水发生反应产生氢气.现将金属钠放入硫酸铜溶液中,该过程中不可能发生的反应是( )
| A、2Na+2H2O=2NaOH+H2↑ |
| B、2Na+CuSO4=Na2SO4+Cu |
| C、4Na+O2=2Na2O |
| D、2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 |


 某化学兴趣小组的同学在老师的指导下,开展如下探究活动.
某化学兴趣小组的同学在老师的指导下,开展如下探究活动.

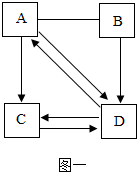
 金属和酸、碱、盐的化学性质是初中化学的核心知识,如图,A、B、C、D分别表示上述四类物质中常见的一种,A、B、C、D之间的连线表示它们彼此之间能够发生化学反应,其中A与B能够发生中和反应,D是目前世界上产量最多的金属.
金属和酸、碱、盐的化学性质是初中化学的核心知识,如图,A、B、C、D分别表示上述四类物质中常见的一种,A、B、C、D之间的连线表示它们彼此之间能够发生化学反应,其中A与B能够发生中和反应,D是目前世界上产量最多的金属.