题目内容
14.金属M与CuSO4溶液反应的化学方程式为2M+3CuSO4═M2 (SO4)3+3Cu.则下列说法错误的是( )| A. | M的金属活动性比Cu强 | B. | 金属M可能是铁 | ||
| C. | 金属M可能是铝 | D. | 反应前后S元素化合价没有变 |
分析 根据化学方程式表示物质间发生反应的事实,可由金属单质与可溶性盐发生置换反应的化学方程式判断反应分类及金属活动性的强弱关系;
由金属活动顺序表,铜处于氢之后,所以处于氢前的活泼金属都可以把铜从硫酸铜溶液置换出来;根据生成物的化学式RSO4,可判断金属R的化合价,而判断金属R的可能.
解答 解:根据金属R与硫酸铜反应的化学方程式:2M+3CuSO4═M2 (SO4)3+3Cu.
A、根据化学方程式可知,金属R的活泼性比Cu要强,故A正确;
B、金属M与CuSO4溶液反应的化学方程式为2M+3CuSO4═M2 (SO4)3+3Cu,故B错误;
C、M在硫酸盐中显+3价,所以金属M可能是铝,故C正确;
D、反应前后S元素化合价都是+6价,故D正确.
故选:B.
点评 本题综合性的考查了有关金属的性质,活动性强的金属可以把活动性弱的金属从其盐溶液中置换出来;根据金属与盐溶液的反应,可以判断反应中两种金属的活动性强弱关系.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列除杂方法错误的是(括号内物质为杂质)( )
| A. | CO2(CO)-通入氧气,点燃 | B. | CO2(O2)-通过灼热的铜网 | ||
| C. | CuO(C粉)-在氧气中加热 | D. | CaO(CaCO3)-高温煅烧 |
5.化学新教材加大了化学实验探究的力度,提高了同学们动手实验的能力,如图所示基本的实验操作不正确的是( )
| A. |  液体体积读数 | B. |  熄灭酒精灯 | C. | 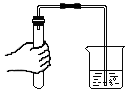 检查气密性 | D. |  滴加液体 |
2.四位同学分别归纳出下列结论:①氧气在一定条件下可转化成臭氧,该变化肯定是物理变化;②物质变色了则一定发生了化学变化;③爆炸不一定是化学变化;④某固态物质在一定条件下观察到放出气体,则一定是发生了化学变化.其中正确的是( )
| A. | ①③ | B. | ②③ | C. | ②④ | D. | ③ |
9.下列化学方程式书写正确的是( )
| A. | 镁带燃烧 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | |
| B. | 双氧水制氧气 H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2↑+O2↑ | |
| C. | C 和CO2反应 CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO | |
| D. | CO还原CuO CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2↑ |
2.水是重要资源,下列说法正确的是( )
| A. | 过滤和煮沸均能使硬水转化为软水 | |
| B. | 活性炭的吸附作用可使海水转化为淡水 | |
| C. | 电解水得到的氢气和氧气的质量比为2:1 | |
| D. | 水通过“三态”变化在自然界中循环 |
6.下列化学反应,属于化合反应的是( )
| A. | NH3+HCl═NH4Cl | B. | 2HgO $\stackrel{△}{→}$2Hg+O2↑ | ||
| C. | CuO+CO$\stackrel{△}{→}$Cu+CO2 | D. | Mg+2HCl═MgCl2+H2↑ |