题目内容
利用海水(含氯化钠、氯化镁)处理含二氧化硫废气的方法如下:
Ⅰ.图1是海水处理流程:
(1)写出生成Mg(OH)2沉淀的化学反应方程式______
(2)经操作a得到的Mg(OH)2沉淀需要洗净,为证明是否洗净,可取洗涤液少量,向其中加入下列试剂中的,即可达到实验目的______.A.Na2CO3溶液 B.石灰水 C.硝酸银溶液
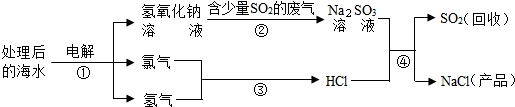
Ⅱ.图2是处理二氧化硫流程:
(3)图中最终得到“NaCl”的过程属于______(填“物理变化”或“化学变化”).
(4)图中反应①、③、④属于化合反应的是______(填序号).
(5)①中反应的化学方程式为______.
(6)④中反应的化学方程式为______.

解:Ⅰ.(1)海水中含氯化钠、氯化镁,氯化镁与石灰水反应可生成Mg(OH)2沉淀,化学反应方程式是:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.
(2)A.Na2CO3溶液 C.硝酸银溶液都可以与CaCl2反应生成沉淀.
Ⅱ.
(3)从海水最终得到“NaCl(产品)”是反应生成的氯化钠,故该变化属于化学变化.
(4)化合反应是多种物质反应生成一种物质,③氯气和氢气反应生成氯化氢的反应属于化合反应,①的生成物是三种属于分解反应,④的反应物生成物是两种化合物,属复分解反应故不是化合反应;
(5)①中的反应物是氯化钠和水生成物是氢气、氯气和氢氧化钠.故答反应的化学方程式为:2NaCl+2H2O 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;
(6)反应④是硫酸氢钠和盐酸反应生成二氧化硫、水和氯化钠的过程,故化学方程式为:NaHSO3+HCl═NaCl+H2O+SO2↑.
故答案为:(1)MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2 .
(2)AC.
(3)化学.
(4)③.
(5)2NaCl+2H2O 2NaOH+2H2↑+Cl2↑.
2NaOH+2H2↑+Cl2↑.
(6)NaHSO3+HCl═NaCl+SO2↑+H2O.
分析:Ⅰ.
(1)氯化镁与石灰水反应可生成Mg(OH)2沉淀.
(2)根据(1)的化学方程式可知,要检验经操作a得到的Mg(OH)2沉淀是否洗净,就要加入能与CaCl2反应生成沉淀的试剂.
Ⅱ.
(3)由题目中的框图可知:从海水最终得到NaCl(产品)的过程可知,每一步都有新物质生成,为化学变化.
(4)根据化合反应的定义判断.
(5)根据反应物、反应条件、生成物写出化学方程式.
(6)根据反应物、反应条件、生成物写出化学方程式.
点评:此题涉及知识点较多,难度较大.
(2)A.Na2CO3溶液 C.硝酸银溶液都可以与CaCl2反应生成沉淀.
Ⅱ.
(3)从海水最终得到“NaCl(产品)”是反应生成的氯化钠,故该变化属于化学变化.
(4)化合反应是多种物质反应生成一种物质,③氯气和氢气反应生成氯化氢的反应属于化合反应,①的生成物是三种属于分解反应,④的反应物生成物是两种化合物,属复分解反应故不是化合反应;
(5)①中的反应物是氯化钠和水生成物是氢气、氯气和氢氧化钠.故答反应的化学方程式为:2NaCl+2H2O
 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;(6)反应④是硫酸氢钠和盐酸反应生成二氧化硫、水和氯化钠的过程,故化学方程式为:NaHSO3+HCl═NaCl+H2O+SO2↑.
故答案为:(1)MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2 .
(2)AC.
(3)化学.
(4)③.
(5)2NaCl+2H2O
 2NaOH+2H2↑+Cl2↑.
2NaOH+2H2↑+Cl2↑.(6)NaHSO3+HCl═NaCl+SO2↑+H2O.
分析:Ⅰ.
(1)氯化镁与石灰水反应可生成Mg(OH)2沉淀.
(2)根据(1)的化学方程式可知,要检验经操作a得到的Mg(OH)2沉淀是否洗净,就要加入能与CaCl2反应生成沉淀的试剂.
Ⅱ.
(3)由题目中的框图可知:从海水最终得到NaCl(产品)的过程可知,每一步都有新物质生成,为化学变化.
(4)根据化合反应的定义判断.
(5)根据反应物、反应条件、生成物写出化学方程式.
(6)根据反应物、反应条件、生成物写出化学方程式.
点评:此题涉及知识点较多,难度较大.

练习册系列答案
相关题目
近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程如下图所示.下列说法正确的是( )


| A、可循环利用的物质是SO2 | B、图中反应①属于分解反应 | C、反应中硫元素的化合价发生变化 | D、从海水中最终得到“NaCl(产品)”的过程是物理变化 |