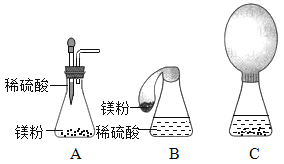
题目内容
【题目】在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前及反应过程中的两个时刻各物质的质量分数如下图所示,图中a、b、c、d分别表示相应物质的质量分数。请写出a的值为:_____,该反应的基本反应类型是:_____;
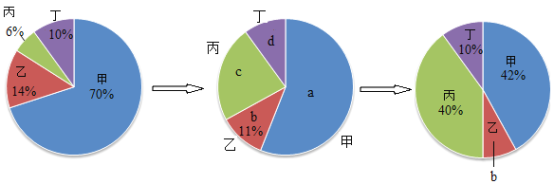
【答案】56% 化合反应
【解析】
反应后质量增多的物质是生成物,质量减少的物质是反应物,差量是生成的质量或参加反应的质量。根据质量守恒定律,反应后乙的含量为:1-40%-10%-42%=8%,设密闭容器中物质的总质量为100g,甲反应后质量减少,甲是反应物,参加反应的甲的质量为:100g×70%-100g×42%=28g,乙反应后质量减少,乙是反应物,参加反应的质量为:100g×14%-100g×8%=6g,丙反应后质量增多,丙是生成物,生成丙的质量为:100g×40%-100g×6%=34g,丁的质量不变,该反应为:甲+乙=丙。反应中甲与乙的质量比为28g:6g,设参加反应的甲的质量为x,则![]() ,解得x=14g,故a=70%-14%=56%,由两种或两种以上的物质发生化学反应生成另一种物质的反应是化合反应,该反应的基本反应类型是化合反应。
,解得x=14g,故a=70%-14%=56%,由两种或两种以上的物质发生化学反应生成另一种物质的反应是化合反应,该反应的基本反应类型是化合反应。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】如图是某学生绘制的元素周期表的一部分:
1H 氢 | 2He 氦 | ||||||
3Li 锂 | 4Be 铍 | 5B 硼 | 6C 炭 | 7N 氮 | 8O 氧 | 9F 氟 | 10Ne 氖 |
11Na 钠 | 12Mg 镁 | 13Al 铝 | 14Si 硅 | 15P 磷 | 16S 硫 | 17Cl 氯 | 18Ar 氩 |
请根据相关信息与知识回答:
(1)原子序数分别为8、13两种元素组成的化合物的化学式是____.
(2)仔细阅读和观察上表,其中有一种常见元素的元素名称书写有误,请写出其正确的元素名称:_____,过量排放该元素的一种氧化物到大气中,会引起____效应,使全球变暖,请列举至少一条防止该效应进一步增强的措施:____.
![]()