题目内容
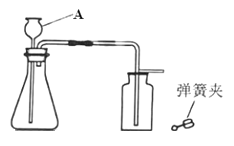
【题目】请根据下列装置回答问题:根据下列实验装置图,按要求回答问题。
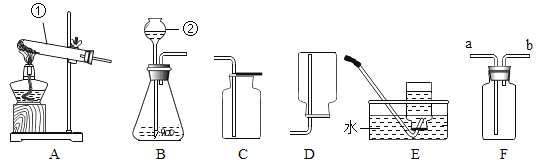
(1)写出标有序号的仪器名称:②_____;
(2)若用氯酸钾制取一瓶纯净的氧气,应选择的装置是_____;用高锰酸钾制取氧气的化学方程式为_____;
(3)小组成员小慧同学想用氯酸钾制取一瓶氧气,误把高锰酸钾当成二氧化锰,加热时氯酸钾的反应速率也很快。于是她惊奇地告诉同学舒展:高锰酸钾也可以作为氯酸钾分解的催化剂。小明经过思考后,认为小慧的结论不科学。你认为高锰酸钾能加快氧酸钾分解的原因是_____;
(4)若用E装置收集氧气时,所收集的氧气不纯的原因可能是_____;用C装置收集氧气时,验满的方法为_____;
(5)一氧化氮在常温下是一种难溶于水的气体,密度比空气略大,能跟空气中的氧气迅速反应,生成二氧化氮。要采用装置F收集一氧化氮气体,简述操作方法_____。
(6)将30.9g氯酸钾(KClO3)和二氧化锰的固体混合物装入试管中,加热制取氧气,同时生成氯化钾。待反应完全后,将试管冷却,称量,可以得到21.3 g固体物质。请计算原固体混合物中氯酸钾的质量_____。
【答案】长颈漏斗 AE ![]() KMnO4分解产生的MnO2可以作为氯酸钾分解的催化剂,使速率加快 没有等到导管口有连续且均匀的气泡冒出便开始收集/集气瓶中未装满水 将带火星的小木条放在集气瓶口,若复燃,则已收集满 将F装置中的集气瓶装满水,然后将NO从b管通入,水从a管排出 24.5g
KMnO4分解产生的MnO2可以作为氯酸钾分解的催化剂,使速率加快 没有等到导管口有连续且均匀的气泡冒出便开始收集/集气瓶中未装满水 将带火星的小木条放在集气瓶口,若复燃,则已收集满 将F装置中的集气瓶装满水,然后将NO从b管通入,水从a管排出 24.5g
【解析】
(1)据图可知仪器②的名称是长颈漏斗;
(2)如果用氯酸钾制氧气就需要加热,应选择的发生装置是A,用排水法能收集到较纯净的氧气,收集装置应用E;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式为![]() ;
;
(3)高锰酸钾能加快氯酸钾分解的原因是:高锰酸钾受热分解时生成了二氧化锰;因此高锰酸钾不是该反应的催化剂,起催化作用的是二氧化锰;
(4)若用E装置收集氧气时,所收集的氧气不纯的原因可能是:没有等到气泡连续、均匀的冒出就收集;集气瓶中的水没有装满等;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;;
(5)一氧化氮在常温下是一种难溶于水的气体,密度比空气略大,能跟空气中的氧气迅速反应,生成二氧化氮,收集一氧化氮气体只能用排水法,要采用装置F收集一氧化氮气体,操作方法为:将F装置中的集气瓶装满水,然后将一氧化氮从b管通入,水从a管排出;
(6)根据质量守恒定律可得,生成的氧气的质量为30.9g-21.3g=9.6g,设原混合物中氯酸钾的质量为x,
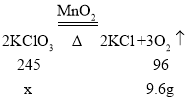
![]()
x=24.5g。

【题目】在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得部分数据如下表:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 18 | 1 | 2 | 32 |
反应后质量/g | X | 26 | 2 | 12 |
下列说法中,正确的是( )
A.反应后物质甲的质量为13g
B.物质丙是该反应的催化剂
C.参加反应的甲和丁的质量之比为9:16
D.![]()