题目内容
2.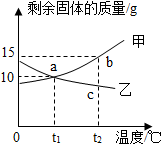 将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体的质量与温度的关系如图所示,下列说法正确的是( )
将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体的质量与温度的关系如图所示,下列说法正确的是( )| A. | 甲的溶解度随温度升高而增大 | |
| B. | t1℃时,甲、乙的溶解度均为20g | |
| C. | a、b、c三点中溶质的质量分数:c>a>b | |
| D. | 温度由t2℃降低到t1℃时,甲溶液析出5g固体 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、随着温度的升高,甲固体逐渐增多,所以甲的溶解度随温度升高而减小,故A错误;
B、t1℃时,剩余固体质量为20g,所以甲、乙的溶解度均为10g,故B错误;
C、通过分析溶解度曲线可知,b处剩余的固体最多,c处剩余的固体最少,所以a、b、c三点中溶质的质量分数:c>a>b,故C正确;
D、温度由t2℃降低到t1℃时,固体减少5g,所以甲溶液溶解5g固体,故D错误.
故选:C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
12.逻辑推理是一种重要的化学思维方法,下列推理合理的是( )
| A. | 铁能与盐酸反应,所以金属都能与酸反应 | |
| B. | 因为氧化物含有氧元素,所以含氧元素的化合物都是氧化物 | |
| C. | Na+、Mg2+、Cl-的最外层电子数均为8,由此得出离子的最外层电子数均为8 | |
| D. | 同温下分解过氧化氢、加催化剂的反应速率快,说明催化剂可以改变反应速率 |
7.下列符号中既能表示物质的元素组成,又能表示该物质的一个分子,正确的是
①Cu ②N ③H2O2 ④K2CO3 ⑤CH4( )
①Cu ②N ③H2O2 ④K2CO3 ⑤CH4( )
| A. | ①② | B. | ③④ | C. | ②④ | D. | ③⑤ |
12.下列科学家与他的贡献对应不正确的是( )
| A. | 侯德榜---联合制碱法 | |
| B. | 门捷列夫---元素周期表 | |
| C. | 阿基米德---杠杆原理:F1l1=F2l2 | |
| D. | 欧姆---电流通过导体产生的热量:Q=I2Rt |
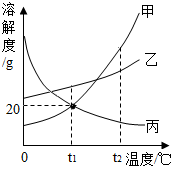 甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示.
甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示.