题目内容
过氧化氢溶液在存放过程中会自然分解,使溶质质量分数减小。某同学使用一瓶原标注为30%的过氧化氢溶液完成制取氧气的实验。通过称量,该瓶中共有116.8 g溶液,取出13.6 g在一定条件下进行实验,发现生成气体的质量与反应时间的关系如右图所示。试计算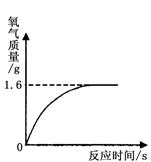
⑴现在这瓶过氧化氢溶液的溶质质量分数。
⑵该瓶溶液中,已经分解的过氧化氢质量。
(1)25%, (2)6.8g
解析试题分析:⑴根据图像可知,13.6g过氧化氢完全反应,生成氧气1.6g;可根据题意书写反应的化学方程式,并找出其中过氧化氢与氧气的质量比,利用氧气的质量即可求出过氧化氢的质量,进而计算出过氧化氢溶液的溶质质量分数。
设13.6g过氧化氢溶液中溶质的质量为x。
2H2O2 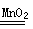 2H2O + O2↑
2H2O + O2↑
68 32
x 1.6g
68:32=x:1.6g
解得,x=3.4g
则该溶液中溶质的质量分数=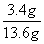 ×100%=25%。
×100%=25%。
⑵根据反应的化学方程式,判断已分解过氧化氢的质量与放出氧气的质量关系,分析久置后溶液的组成,由上一步所计算的溶液的溶质质量分数,求出已经分解的过氧化氢质量。
设已分解的过氧化氢的质量为y ,产生氧气的质量为z。
2H2O2 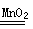 2H2O + O2↑
2H2O + O2↑
68 32
y z
z=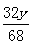
则有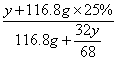 =30%
=30%
解得,y=6.8g
答:⑴现在这瓶过氧化氢溶液的溶质质量分数为25%。⑵该瓶溶液中,已经分解的过氧化氢质量为6.8g。
考点:有关溶质质量分数的简单计算,根据化学反应方程式的计算
点评:此题是关于化学方程式的计算题,主要是利用图表及反应方程式来分析和解决化学计算中的有关问题,要求学生有较强的数据分析能力;解题的关键是要明确久置后的溶液的组成,以及已分解过氧化氢的质量与放出氧气的质量关系。

 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 过氧化氢溶液在存放过程中会缓慢分解.右图为实验室保存的一瓶过氧化氢溶液的标签.某小组同学为了解过氧化氢的分解情况,取5g该溶液共制得0.64g氧气.试分析计算
过氧化氢溶液在存放过程中会缓慢分解.右图为实验室保存的一瓶过氧化氢溶液的标签.某小组同学为了解过氧化氢的分解情况,取5g该溶液共制得0.64g氧气.试分析计算
 (2013?丰台区一模)过氧化氢溶液在存放过程中会自然分解,使溶质质量分数减小.某同学使用一瓶原标注为30%的过氧化氢溶液完成制取氧气的实验.通过称量,该瓶中共有116.8g溶液,取出13.6g在一定条件下进行实验,发现生成气体的质量与反应时间的关系如图所示.试计算
(2013?丰台区一模)过氧化氢溶液在存放过程中会自然分解,使溶质质量分数减小.某同学使用一瓶原标注为30%的过氧化氢溶液完成制取氧气的实验.通过称量,该瓶中共有116.8g溶液,取出13.6g在一定条件下进行实验,发现生成气体的质量与反应时间的关系如图所示.试计算 过氧化氢溶液在存放过程中会缓慢分解.如图是实验室保存的一瓶过氧化氢溶液.某小组16学为了解过氧化氢的分解情况,取10g该溶液共制得1.28g氧气.试分析计算这瓶过氧化氢溶液在保存过程中已经分解的过氧化氢的质量.
过氧化氢溶液在存放过程中会缓慢分解.如图是实验室保存的一瓶过氧化氢溶液.某小组16学为了解过氧化氢的分解情况,取10g该溶液共制得1.28g氧气.试分析计算这瓶过氧化氢溶液在保存过程中已经分解的过氧化氢的质量. 过氧化氢溶液在存放过程中会缓慢分解.如图为某校实验室保存的一瓶过氧化氢溶液的标签.某小组同学为了解过氧化氢的分解情况,将该瓶溶液全部用于制取氧气,测得其共放出气体32g(不考虑水分的蒸发),求剩余溶液中溶质质量分数.
过氧化氢溶液在存放过程中会缓慢分解.如图为某校实验室保存的一瓶过氧化氢溶液的标签.某小组同学为了解过氧化氢的分解情况,将该瓶溶液全部用于制取氧气,测得其共放出气体32g(不考虑水分的蒸发),求剩余溶液中溶质质量分数.