题目内容
 锌(Zn)与盐酸(HCl)反应生成氯化锌(ZnCl2)和氢气.生成氢气的质量与反应时间的关系如图所示:
锌(Zn)与盐酸(HCl)反应生成氯化锌(ZnCl2)和氢气.生成氢气的质量与反应时间的关系如图所示:(1)完全反应后生成氢气的质量为
0.4g
0.4g
;(2)试计算参加反应的锌的质量?
分析:(1)根据图示知,当氢气的质量是0.4g时,氢气的质量不再变化,据此可以得到完全反应后生成的氢气的质量;
(2)根据化学方程式找出锌与氢气的质量比,由氢气的质量可计算出参加反应的锌的质量.
(2)根据化学方程式找出锌与氢气的质量比,由氢气的质量可计算出参加反应的锌的质量.
解答:解:(1)根据图示知,当氢气的质量为0.4g时,氢气的质量不再发生变化,即该反应完全反应后生成氢气的质量是0.4g.
故填:0.4g;
(2)设参加反应锌的质量为x.
Zn+2HCl=ZnCl2+H2↑
65 2
x 0.4g
则
=
解得,x=13 g
答:参加反应锌的质量为13g.
故填:0.4g;
(2)设参加反应锌的质量为x.
Zn+2HCl=ZnCl2+H2↑
65 2
x 0.4g
则
| 65 |
| x |
| 2 |
| 0.4g |
解得,x=13 g
答:参加反应锌的质量为13g.
点评:本题是借助于数学模型,利用平面直角坐标系中的曲线来分析和解决化学计算中的有关问题,要求学生有较强的识图能力和数据分析能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
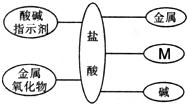 (2010?陕西)构建知识网络,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的知识网络.
(2010?陕西)构建知识网络,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的知识网络. 27、用下列仪器和试剂验证影响金属与盐酸反应速率的因素:烧杯、试管夹、酒精灯、药匙、量筒、天平.锌片、铁片、镁片.5%盐酸、20%盐酸.
27、用下列仪器和试剂验证影响金属与盐酸反应速率的因素:烧杯、试管夹、酒精灯、药匙、量筒、天平.锌片、铁片、镁片.5%盐酸、20%盐酸.
 将A、B、C和锌四种金属分别同时放入稀盐酸中,小明将观察到的现象形象的画了一幅卡通画,每个卡通人物表示一种金属,周围的小黑点表示反应中生成的气体.问:
将A、B、C和锌四种金属分别同时放入稀盐酸中,小明将观察到的现象形象的画了一幅卡通画,每个卡通人物表示一种金属,周围的小黑点表示反应中生成的气体.问: