题目内容
取25克石灰石样品,放在盛有125克稀盐酸的烧杯中,恰好完全反应(杂质不参加反应),烧杯内物质质量变为141.2克,求:(1)生成CO2的质量;
(2)石灰石样品的纯度.
【答案】分析:(1)根据该反应中只有二氧化碳是气体,则利用质量守恒定律和反应前后烧杯中物质的总质量之差来计算二氧化碳的质量;
(2)将二氧化碳的质量代入化学反应方程式来计算碳酸钙的质量,再计算碳酸钙的质量分数;
解答:解:(1)由质量守恒可知,二氧化碳的质量为25g+125g-141.2g=8.8g,
(2)设反应中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 8.8g
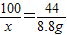
解得x=20g
该样品中碳酸钙的质量分数为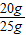 ×100%=80%,
×100%=80%,
答:(1)反应生成二氧化碳的质量是8.8g;(2)石灰石中含碳酸钙的质量分数为80%.
点评:本题考查学生利用化学反应方程式的计算,明确二氧化碳是气体并利用质量守恒来计算二氧化碳的质量是解答的关键.
(2)将二氧化碳的质量代入化学反应方程式来计算碳酸钙的质量,再计算碳酸钙的质量分数;
解答:解:(1)由质量守恒可知,二氧化碳的质量为25g+125g-141.2g=8.8g,
(2)设反应中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 8.8g
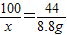
解得x=20g
该样品中碳酸钙的质量分数为
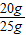 ×100%=80%,
×100%=80%,答:(1)反应生成二氧化碳的质量是8.8g;(2)石灰石中含碳酸钙的质量分数为80%.
点评:本题考查学生利用化学反应方程式的计算,明确二氧化碳是气体并利用质量守恒来计算二氧化碳的质量是解答的关键.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目