题目内容
小明发现实验室一瓶氢氧化钠瓶盖已经打开,小明推测该瓶氢氧化钠已经变质,其变质的原因是 ,反应的方程式为 ,可以用 检验其是否变质,反应的方程式为 ,如果变质应用 除去其中的杂质,反应方程式为 .小明推测瓶中物质为碳酸钠,但小华认为还有可能是 .请你帮助设计实验验证该瓶的成分.
考点:碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:氢氧化钠放置在空气中易与空气中的二氧化碳发生化学反应,生成碳酸钠,如果装置不密封,可以导致药品变质,因产物中含有碳酸根离子,因此检验方法实际就是检验溶液中碳酸根离子的存在,常用加稀盐酸的方法,另外还可以用沉淀法判断碳酸根离子的存在,可用含Ca2+或Ba2+溶液,滴加到样品中,若出现白色沉淀,则说明原溶液中含有碳酸根离子,也就是原药品变质.
对于变质的氢氧化钠,我们还可以采用上述沉淀法将其杂质离子除去,而得到纯净的氢氧化钠溶液,方法是加入适量氢氧化钙溶液,钙离子与原溶液中的碳酸根离子结合生成碳酸钙白色沉淀,即可过滤除掉.
对于变质的氢氧化钠,我们还可以采用上述沉淀法将其杂质离子除去,而得到纯净的氢氧化钠溶液,方法是加入适量氢氧化钙溶液,钙离子与原溶液中的碳酸根离子结合生成碳酸钙白色沉淀,即可过滤除掉.
解答:解:氢氧化钠放置在空气中易与空气中的二氧化碳发生化学反应,生成碳酸钠,而使氢氧化钠变质.故答案应为:CO2+2NaOH═Na2CO3+H2O.检验是否变质,就是看溶液中是不是已经存在了碳酸根离子,检验溶液中碳酸根离子的存在,常用加稀盐酸的方法,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.如果变质应用氢氧化钙除去其中的杂质,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,验证有碳酸钠存在,还可能是氢氧化钠与碳酸钠的混合物.如果氢氧化钠全部变质,则全部生成了碳酸钠,所以可以在排除碳酸钠干扰的条件下来验证是否含有氢氧化钠即可,故可以选择加入足量的氯化钙溶液,将碳酸钠转化为沉淀,然后来测定用无色酚酞来测定溶液的酸碱性即可得出结论.
故答案为:氢氧化钠与空气中的二氧化碳发生化学反应,生成碳酸钠,而使氢氧化钠变质;CO2+2NaOH═Na2CO3+H2O;稀盐酸;Na2CO3+2HCl═2NaCl+H2O+CO2↑;氢氧化钙;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;氢氧化钠与碳酸钠的混合物;
实验步骤:①取少量该氢氧化钠溶液于试管中,加入足量CaCl2溶液;
②过滤,在滤液中滴加无色酚酞试液;
实验现象:①有白色沉淀生成;
②溶液变红;
实验结论:该氢氧化钠溶液部分变质,是氢氧化钠与碳酸钠的混合物.
故答案为:氢氧化钠与空气中的二氧化碳发生化学反应,生成碳酸钠,而使氢氧化钠变质;CO2+2NaOH═Na2CO3+H2O;稀盐酸;Na2CO3+2HCl═2NaCl+H2O+CO2↑;氢氧化钙;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;氢氧化钠与碳酸钠的混合物;
实验步骤:①取少量该氢氧化钠溶液于试管中,加入足量CaCl2溶液;
②过滤,在滤液中滴加无色酚酞试液;
实验现象:①有白色沉淀生成;
②溶液变红;
实验结论:该氢氧化钠溶液部分变质,是氢氧化钠与碳酸钠的混合物.
点评:本题以变质的氢氧化钠溶液引题,考查变质原因,会书写化学方程式,结合检验方法,解题思路比较灵活,既能考查氢氧化钠和碳酸盐的性质,碳酸根的检验和碳酸盐杂质的除去,又考查了像过滤、搅拌等实验操作,考查面较广,不错的一道题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于氧气的物质性质的叙述,正确的是( )
| A、液态氧是无色的液体 |
| B、鱼儿能在水中生存,说明氧气易溶于水 |
| C、氧气的密度比空气的密度略小 |
| D、通常状况,氧气是无色无味的气体 |
0.5L 1mol/L的FeCl3溶液与0.2L 1mol/L的KCl溶液中,Cl-浓度比为( )
| A、15:2 | B、1:1 |
| C、3:1 | D、1:3 |
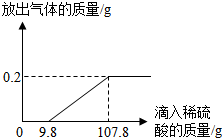 在烧杯中加入久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示(该反应中的化学方程式有Al2O3+3H2SO4═Al2(SO4)3+3H2O、2Al+3H2SO4═Al2(SO4)3+3H2↑)请回答下列问题:
在烧杯中加入久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示(该反应中的化学方程式有Al2O3+3H2SO4═Al2(SO4)3+3H2O、2Al+3H2SO4═Al2(SO4)3+3H2↑)请回答下列问题: