题目内容
能在pH为3的溶液中大量共存,且溶液为无色透明的一组物质是( )A.BaCl2、NaOH
B.K2SO4、NaCl
C.CaCl2、Na2CO3
D.CuSO4、KCl
解答:解:pH为3的水溶液显酸性,水溶液中含有大量的H+.
A、NaOH中的氢氧根离子和和H+在溶液中能结合生成水,不能大量共存,故选项错误.
B、K2SO4、NaCl在溶液中相互交换成分不能生成沉淀、气体、水,能在酸性溶液中大量共存,故选项正确.
C、Na2CO3和H+在溶液中能结合生成水和二氧化碳,不能大量共存,故选项错误.
D、两者之间不反应,且能在酸性溶液中共存,但CuSO4溶于水呈蓝色,故选项错误.
故选B.
点评:本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水;还要注意在酸性溶液中共存及特定离子的颜色.

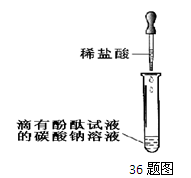
(4分)张南同学为了验证Na2CO3溶液中的碳酸根离子,做了如下实验。操作如下:

①向一支试管中加入约3mL的Na2CO3溶液,并滴入2滴酚酞试液,振荡试管,溶液呈均匀的红色;
②再向此试管中逐滴加入稀盐酸,至溶液颜色由红色恰好变为无色。
<提出问题>为什么向Na2CO3溶液中滴加稀盐酸不产生气泡?
<猜想与假设>(提示:试剂没有问题)
①Na2CO3溶液和稀盐酸没有发生化学反应。
②Na2CO3溶液和稀盐酸发生化学反应生成的二氧化碳溶于水。
③Na2CO3溶液和稀盐酸发生化学反应生成的产物不是二氧化碳。
资料:①此Na2CO3溶液的pH 约为11,NaHCO3溶液的pH约为8;
②NaHCO3在水溶液中受热不分解;
③酚酞试液在pH≥10时的溶液为红色,在pH≤8.2时溶液为无色;
<设计方案及实验>经过讨论大家首先否定了猜想①,其理由是 。
对方案②和③进行研究,决定进行如下实验,首先把上述反应后的溶液分装成3支试管。请 完 成下列表格。
| 编号 | 方案 | 实验步骤 | 预期现象 | 实验结论 |
| 猜想② | 利用CO2的溶解度受温度的升高而溶解度降低,给试管加热,用石灰水检验产生的气体。 | 取其中的1支试管,在酒精灯上加热,再将产生的气体通入石灰水。 | 产生白色沉淀
结果没有产生上述现象 |
则猜想②不成立 |
|
猜想③
| 加入酸的量不足,继续加酸。 | 取其中的另1支试管,再继续滴加稀盐酸。 |
| 猜想③成立 |
<解释与结论>张南同学开始时的实验,即向Na2CO3溶液中滴加稀盐酸没有看到气泡的原因是(写方程式) 。
<反思与应用>(1)在不另取其他试剂的情况下,能够鉴别Na2CO3溶液和稀盐酸两种溶液吗? (填“能’ ”或“不能”)。
(2)有些化学反应的产物与 有关。

①向一支试管中加入约3mL的Na2CO3溶液,并滴入2滴酚酞试液,振荡试管,溶液呈均匀的红色;
②再向此试管中逐滴加入稀盐酸,至溶液颜色由红色恰好变为无色。
<提出问题>为什么向Na2CO3溶液中滴加稀盐酸不产生气泡?
<猜想与假设>(提示:试剂没有问题)
①Na2CO3溶液和稀盐酸没有发生化学反应。
②Na2CO3溶液和稀盐酸发生化学反应生成的二氧化碳溶于水。
③Na2CO3溶液和稀盐酸发生化学反应生成的产物不是二氧化碳。
资料:①此Na2CO3溶液的pH 约为11,NaHCO3溶液的pH约为8;
②NaHCO3在水溶液中受热不分解;
③酚酞试液在pH≥10时的溶液为红色,在pH≤8.2时溶液为无色;
<设计方案及实验>经过讨论大家首先否定了猜想①,其理由是 。
对方案②和③进行研究,决定进行如下实验,首先把上述反应后的溶液分装成3支试管。请 完 成下列表格。
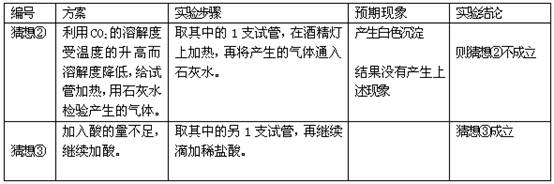
| 编号 | 方案 | 实验步骤 | 预期现象 | 实验结论 |
| 猜想② | 利用CO2的溶解度受温度的升高而溶解度降低,给试管加热,用石灰水检验产生的气体。 | 取其中的1支试管,在酒精灯上加热,再将产生的气体通入石灰水。 | 产生白色沉淀 结果没有产生上述现象 | 则猜想②不成立 |
| 猜想③ | 加入酸的量不足,继续加酸。 | 取其中的另1支试管,再继续滴加稀盐酸。 | | 猜想③成立 |
<反思与应用>(1)在不另取其他试剂的情况下,能够鉴别Na2CO3溶液和稀盐酸两种溶液吗? (填“能’ ”或“不能”)。
(2)有些化学反应的产物与 有关。