题目内容
氯化钙钾石的化学式为KCl·xCaCl2(x是CaCl2的系数)。它是一种钾肥,溶于水后得到KCl和CaCl2的混合溶液。某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液210g,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如下图所示。
已知:Na2CO3 + CaCl2 ![]() CaCO3↓ + 2NaCl
CaCO3↓ + 2NaCl
请计算:
(1) 氯化钙钾石中钾元素的质量分数。
(2) B点时溶液中Na2CO3的质量分数。
 |
【解】设CaCl2的质量为x,A点时参加反应的Na2CO3的质量为y
Na2CO3+ CaCl2 CaCO3+ 2NaCl
106 111 100
y x 10g
x = ![]() =11.1 g
=11.1 g
y = ![]() =10.6 g
=10.6 g
KCl的质量=18.55 g - 11.1g = 7.45 g
氯化钙钾石中钾元素的质量分数=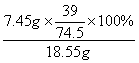 ×100% = 21.0%
×100% = 21.0%
所加Na2CO3溶液的质量分数=![]() ×100%=10%
×100%=10%
B点时的溶液中Na2CO3的质量分数=![]() ×100% = 2.4%-
×100% = 2.4%-
答:氯化钙钾石中钾元素的质量分数为21.0% ,B点时溶液中Na2CO3的质量分数2.4%。

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
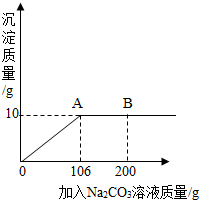 氯化钙钾石的化学式为KCl?xCaCl2(x是CaCl2的系数).它是一种天然的钾肥,溶于水后得到KCl与CaCl2的混合溶液.某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如右图所示.请回答下列问题:
氯化钙钾石的化学式为KCl?xCaCl2(x是CaCl2的系数).它是一种天然的钾肥,溶于水后得到KCl与CaCl2的混合溶液.某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如右图所示.请回答下列问题: (2012?昌平区一模)氯化钙钾石的化学式为KCl?xCaCl2(x是CaCl2的系数).它是一种钾肥,溶于水后得到KCl和CaCl2的混合溶液.某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液210g,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如图所示.已知:Na2CO3+CaCl2═CaCO3↓+2NaCl,请计算:
(2012?昌平区一模)氯化钙钾石的化学式为KCl?xCaCl2(x是CaCl2的系数).它是一种钾肥,溶于水后得到KCl和CaCl2的混合溶液.某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液210g,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如图所示.已知:Na2CO3+CaCl2═CaCO3↓+2NaCl,请计算:

