题目内容
10.化学实验是科学探究的重要途径.Ⅰ.请根据下列实验图示(图1)回答相关问题:

(1)A实验中,烧杯③的作用是对比.
(2)B实验中,用手握紧试管,观察到导管口出现气泡,说明装置不漏气.
(3)C实验中,装置有错误,改正的方法是长颈漏斗末端伸入液面以下.
(4)D实验中,若要除去粗盐中难溶性的杂质,其正确操作步骤为①④⑤(填序号),步骤⑤中玻璃棒的作用是使液体均匀受热,若要配制50g16%的氯化钠溶液,需要称量8g氯化钠,若按照图②③①的步骤,所配制溶液的溶质质量分数偏大(填“偏大”或“偏小”).
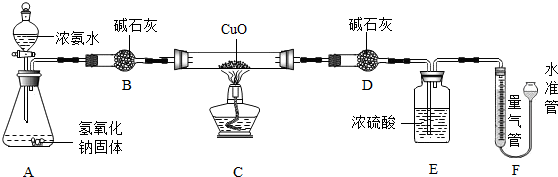
Ⅱ.有一无色气体,可能是由CO、CO2、H2O(水蒸气)中的一种或几种组成.为确定其成分,小明同学按下列方案进行实验(图2),请回答下例问题.

(1)若A中玻璃管内物质由黑色变成红色,则原无色气体中一定含有CO.
(2)若看见B中白色固体不变色现象,则无色气体中一定不含有水蒸气.
(3)若看见澄清石灰水变浑浊,写出C装置中的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
分析 Ⅰ.(1)A实验中,烧杯③的作用是进行对比;
(2)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
(3)为了防止气体从长颈漏斗逸出,长颈漏斗末端应该浸没在液面以下;
(4)过滤能够把不溶于水的固体除去;
Ⅱ.加热条件下,氧化铜和一氧化碳反应生成铜和二氧化碳;
二氧化碳能使澄清石灰水变浑浊.
解答 解:(1)A实验中,烧杯③的作用是对比.
故填:对比.
(2)B实验中,用手握紧试管,观察到导管口出现气泡,说明装置不漏气.
故填:导管口出现气泡.
(3)C实验中,装置有错误,改正的方法是长颈漏斗末端伸入液面以下.
故填:长颈漏斗末端伸入液面以下.
(4)D实验中,若要除去粗盐中难溶性的杂质,其正确操作步骤为①④⑤;
步骤⑤中玻璃棒的作用是使液体均匀受热;
若要配制50g16%的氯化钠溶液,需要氯化钠质量为:50g×16%=8g;
若按照图②③①的步骤,利用量筒量取的水体积偏小,导致所配制溶液的溶质质量分数偏大.
故填:①④⑤;使液体均匀受热;8;偏大.
Ⅱ.(1)若A中玻璃管内物质由黑色变成红色,则原无色气体中一定含有CO.
故填:CO.
(2)若看见B中白色固体不变色,则无色气体中一定不含有水蒸气.
故填:B中白色固体不变色.
(3)二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:Ca(OH)2+CO2═CaCO3↓+H2O.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
20.化学兴趣小组的同学在老师的指导下,开展如下探究活动.
探究一:A、B、C、D分别是纯碱、烧碱、氯化钠、硫酸钠中的一种,它们之间的转化关系如图1所示.
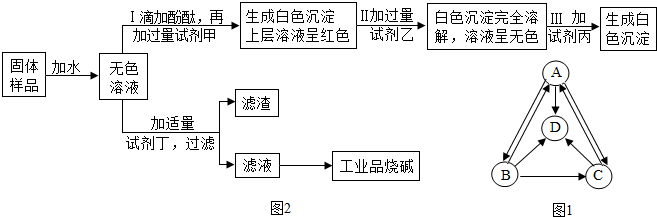
(1)四种物质中,属于碱的是NaOH(填化学式,下同).
(2)物质B是Na2CO3.
探究二:工业品烧碱含有少量氯化钠杂质.该小组同学从一瓶久置的工业品烧碱样品中取出一定量,在烧杯中加适量水溶解后得到样品溶液.用稀硫酸与样品溶液做中和反应实验.有关实验操作和现象如下:
该小组同学对于实验所得红色溶液很感兴趣,展开讨论.溶液里的中和反应是否已经完成?一部分同学认为还没有完成,理由是操作Ⅱ后“溶液仍呈红色”;而另一部分同学则认为中和反应已经完成.结果经过师生共同讨论,确认溶液里中和反应已经完成.
(3)样品溶液的pH>7(填写“<、=或>”).
(4)确认溶液里中和反应已经完成所依据的现象是滴加一定量稀硫酸后溶液中开始产生气泡.
最后,他们设计一个实验方案,验证了久置的工业品烧碱样品中确实含有氯化钠杂质且已经部分变质,并提纯工业品烧碱.其实验流程及部分实验现象如图2所示.
(5)试剂甲和试剂乙的溶液中阴离子都是NO3-(填离子符号).
(6)试剂丁是Ca(OH)2(填化学式).
(7)证明工业品烧碱样品已经部分变质的证据是操作中加过量Ba(NO3)2后生成白色沉淀,上层清液仍呈红色.
探究一:A、B、C、D分别是纯碱、烧碱、氯化钠、硫酸钠中的一种,它们之间的转化关系如图1所示.

(1)四种物质中,属于碱的是NaOH(填化学式,下同).
(2)物质B是Na2CO3.
探究二:工业品烧碱含有少量氯化钠杂质.该小组同学从一瓶久置的工业品烧碱样品中取出一定量,在烧杯中加适量水溶解后得到样品溶液.用稀硫酸与样品溶液做中和反应实验.有关实验操作和现象如下:
| 实验步骤 | 实验现象 |
| Ⅰ.向样品溶液中滴加酚酞溶液 | 溶液呈红色 |
| Ⅱ.向样品溶液中滴加稀硫酸, 并用玻璃棒搅拌 | 滴加一定量稀硫酸后溶液中开始产生气泡 溶液仍呈红色 |
(3)样品溶液的pH>7(填写“<、=或>”).
(4)确认溶液里中和反应已经完成所依据的现象是滴加一定量稀硫酸后溶液中开始产生气泡.
最后,他们设计一个实验方案,验证了久置的工业品烧碱样品中确实含有氯化钠杂质且已经部分变质,并提纯工业品烧碱.其实验流程及部分实验现象如图2所示.
(5)试剂甲和试剂乙的溶液中阴离子都是NO3-(填离子符号).
(6)试剂丁是Ca(OH)2(填化学式).
(7)证明工业品烧碱样品已经部分变质的证据是操作中加过量Ba(NO3)2后生成白色沉淀,上层清液仍呈红色.
2.水是生命之源,下列有关水的说法错误的是( )
| A. | 水是一种重要的溶剂 | |
| B. | 用肥皂水可以区分硬水和软水 | |
| C. | 生活污水毫无用处 | |
| D. | 生活中可以用煮沸的方法降低水的硬度 |
19.科学家正在积极探索利用太阳能分解水来获得氢能源,以解决人类面临的能源危机,从化学反应的基本类型分析,该反应是( )
| A. | 分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 复分解反应 |
20.中华民族辉煌的创造发明史,为世界文明做出了巨大贡献.下列发明创造不涉及化学反应的是( )
| A. | 火药及使用 | B. | 打磨磁石制指南针 | ||
| C. | 用粮食酿酒 | D. | 铁的冶炼 |
 已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答:
已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答: