题目内容
不纯的硝酸铵(NH4NO3)样品,经化学分析,氮元素的质量分数为34.3%(其他杂质不含氮元素),则这种样品含硝酸铵的质量分数是 ,某赤铁矿10g,经实验分析知其含3gFe2O3,则该铁矿石中铁的质量分数为 .
考点:化合物中某元素的质量计算
专题:化学式的计算
分析:根据题意,不纯的硝酸铵(NH4NO3)样品中氮元素的质量分数为34.3%,据此结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:不纯的硝酸铵(NH4NO3)样品,经化学分析,氮元素的质量分数为34.3%(其他杂质不含氮元素),则这种样品含硝酸铵的质量分数是34.3%÷(
×100%)=98%.
某赤铁矿10g,经实验分析知其含3gFe2O3,其中含铁元素的质量为3g×
×100%=2.1g;则该铁矿石中铁的质量分数为
×100%=21%.
故答案为:98%;21%.
| 14×2 |
| 14×2+1×4+16×3 |
某赤铁矿10g,经实验分析知其含3gFe2O3,其中含铁元素的质量为3g×
| 56×2 |
| 56×2+16×3 |
| 2.1g |
| 10g |
故答案为:98%;21%.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
下列说法正确的是( )
| A、通常情况下水是无色的液体 |
| B、无色的液体一定是水 |
| C、只要是无色的液体,就一定能够饮用解渴 |
| D、水蒸发属于物理变化 |
分子、原子的主要区别是( )
| A、分子大,原子小 |
| B、在化学反应中分子可分,原子不可分 |
| C、分子可以构成物质,原子不能构成物质 |
| D、分子是在不断运动着,原子是静止的 |
以下金属活动性最不活泼的是( )
| A、镁 | B、锌 | C、铁 | D、铜 |
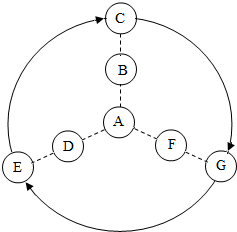 如图表示初中常见几种不同化合物之间的关系,图中“…”表示虚线两边的化合物可以转化或相互反应.请根据以下每小题的具体情况进行解答.
如图表示初中常见几种不同化合物之间的关系,图中“…”表示虚线两边的化合物可以转化或相互反应.请根据以下每小题的具体情况进行解答.