题目内容
10.甲醇(CH3OH)是一种有毒、有酒味的可燃性气体,甲醇在氧气中不完全燃烧可发生如下发应:8CH3OH+nO2═6CO2+2CO+16H2O,若反应生成3.6g水,请计算:(1)n值是11.
(2)参加反应的氧气质量是多少克?
分析 (1)根据化学反应前后,元素的种类不变,原子的种类、总个数不变,原子质量不变,由生成物氧原子总数和甲醇中氧原子总数可以求出n=11;
(2)根据方程式中可以找出参加反应的氧气和生成水的质量比,再由生成水的质量可以求得参加反应的氧气质量.
解答 解:(1)由8CH3OH+nO2$\frac{\underline{\;点燃\;}}{\;}$6CO2 +2CO+16H2O可知,反应后氧原子个数为:12+2+16=30,根据质量守恒定律可知,反应前的氧原子个数也是30个,因此n=$\frac{30-8}{2}$=11,甲醇在氧气中不完全燃烧的化学方程式为:8CH3OH+11O2$\frac{\underline{\;点燃\;}}{\;}$6CO2 +2CO+16H2O;
(2)设参加反应的氧气质量为x
8CH3OH+11O2$\frac{\underline{\;点燃\;}}{\;}$6CO2+2CO+16H2O
11×32 16×18
x 3.6g
$\frac{11×32}{x}$=$\frac{16×18}{3.6g}$
x=4.4g
故答案为:(1)11;
(2)参加反应的氧气质量是4.4g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
20.水是生命之源,下列关于水说法均正确的一组是( )
①用肥皂水鉴别硬水和软水;
②冰由氧元素和氢元素组成;
③用滤纸过滤可以除去水中的所有杂质;
④电解水时生成的氢气和氧气的质量比为2:1;
⑤保持水化学性质的最小微粒是氢分子;
⑥用活性炭可以将硬水软化;
⑦净化水的方法中,蒸馏是单一净化程度最高的;
⑧水是由氢分子和氧原子组成的;
⑨活性炭可除去水中部分不溶性杂质和异味、色素等.
①用肥皂水鉴别硬水和软水;
②冰由氧元素和氢元素组成;
③用滤纸过滤可以除去水中的所有杂质;
④电解水时生成的氢气和氧气的质量比为2:1;
⑤保持水化学性质的最小微粒是氢分子;
⑥用活性炭可以将硬水软化;
⑦净化水的方法中,蒸馏是单一净化程度最高的;
⑧水是由氢分子和氧原子组成的;
⑨活性炭可除去水中部分不溶性杂质和异味、色素等.
| A. | ①②③⑧ | B. | ⑤②①④ | C. | ⑨①②⑦ | D. | ⑥④⑤③ |
18.以下说法不正确的是( )
①有单质和化合物生成的反应一定是置换反应;
②通过化合、分解、置换和复分解反应均可制得二氧化碳;
③凡均一、稳定、透明、澄清的液体一定是溶液;
④棉花、羊毛、塑料和天然橡胶等均属于天然有机高分子材料.
①有单质和化合物生成的反应一定是置换反应;
②通过化合、分解、置换和复分解反应均可制得二氧化碳;
③凡均一、稳定、透明、澄清的液体一定是溶液;
④棉花、羊毛、塑料和天然橡胶等均属于天然有机高分子材料.
| A. | ①② | B. | ①③④ | C. | ③④ | D. | ①②③④ |
15.下列属于纯净物的是( )
| A. | 钛合金 | B. | 水银 | C. | 天然气 | D. | 赤铁矿 |
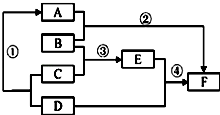 如图是初中化学中六种常见物质之间的转化关系图.已知A、D、F均为单质,其中D、F为金属单质,D的是生产和使用量最多的金属材料;B为黑色氧化物,C是一种常见的酸,E(相对分子质量为160)的溶液呈蓝色.试回答下列问题:(框图中的反应条件和某些生成物已略去)
如图是初中化学中六种常见物质之间的转化关系图.已知A、D、F均为单质,其中D、F为金属单质,D的是生产和使用量最多的金属材料;B为黑色氧化物,C是一种常见的酸,E(相对分子质量为160)的溶液呈蓝色.试回答下列问题:(框图中的反应条件和某些生成物已略去)