题目内容
 某学校的学习小组对当地的石灰石矿区进行调查.与测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品40g,现将100g盐酸分成五等份,逐次加到样品中(假设其他成分不与盐酸反应也不溶于水),得到部分数据与图象如下,
某学校的学习小组对当地的石灰石矿区进行调查.与测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品40g,现将100g盐酸分成五等份,逐次加到样品中(假设其他成分不与盐酸反应也不溶于水),得到部分数据与图象如下,| 第1次 | 第3次 | 第4次 | |
| 加入盐酸质量(g) | 20 | 20 | 20 |
| 剩余固体质量(g) | 35 | a | 20 |
(1)该样品中CaCO3质量分数是
(2)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).
(3)求第五次反应后所得溶液中溶质的质量分数(写出计算过程,计算结果保留一位小数).
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据图象和表格中的数据进行分析解答;
(2)根据二氧化碳的质量求出80g盐酸中氯化氢的质量,进而求质量分数;
(3)根据二氧化碳的质量求出氯化钙的质量,进而求质量分数.
(2)根据二氧化碳的质量求出80g盐酸中氯化氢的质量,进而求质量分数;
(3)根据二氧化碳的质量求出氯化钙的质量,进而求质量分数.
解答:解:(1)由图象可知,在加入80g盐酸后,恰好反应,故第四次加入稀盐酸后,剩余固体为20g,所以样品中碳酸钙的质量为:40g-20g=20g;所以样品中碳酸钙的质量分数为:
×100%=50%;
由第一次加入20g稀盐酸固体质量减少40g-35g=5g,所以结合图象中的信息可知:第三次加入20g盐酸后,所剩固体的质量=35g-5g-5g=25g;
故填:50%;25;
(2)设80g盐酸中氯化氢的质量为x,生成氯化钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 111 44
x y 8.8g
=
=
x=14.6g,y=22.2g
盐酸中溶质的质量分数为:
×100%=18.3%;
答:盐酸中溶质的质量分数为18.3%;
(3)第五次反应后所得溶液中溶质的质量分数为:
×100%=20%
答:第五次反应后所得溶液中溶质的质量分数为20%.
| 20g |
| 40g |
由第一次加入20g稀盐酸固体质量减少40g-35g=5g,所以结合图象中的信息可知:第三次加入20g盐酸后,所剩固体的质量=35g-5g-5g=25g;
故填:50%;25;
(2)设80g盐酸中氯化氢的质量为x,生成氯化钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 111 44
x y 8.8g
| 73 |
| x |
| 111 |
| y |
| 44 |
| 8.8g |
x=14.6g,y=22.2g
盐酸中溶质的质量分数为:
| 14.6g |
| 80g |
答:盐酸中溶质的质量分数为18.3%;
(3)第五次反应后所得溶液中溶质的质量分数为:
| 22.2g |
| 20g+100g-8.8g |
答:第五次反应后所得溶液中溶质的质量分数为20%.
点评:会正确分析图象及表格数据是正确本题的关键.

练习册系列答案
相关题目
下列气体中,在焊接金属时常用的保护气是( )
| A、氢气 | B、氧气 | C、空气 | D、氮气 |
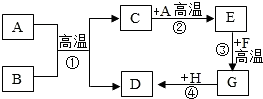
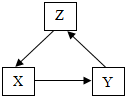 归纳总结是学习化学的一种方法.某同学发现X、Y、Z三种物质有如图所示的循环转化关系,“→”表示能转化.
归纳总结是学习化学的一种方法.某同学发现X、Y、Z三种物质有如图所示的循环转化关系,“→”表示能转化.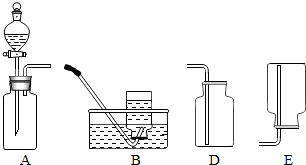 某化学兴趣小组对气体的实验室制法进行了探究.
某化学兴趣小组对气体的实验室制法进行了探究.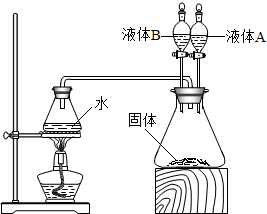 如图所示,用酒精灯给锥形瓶中的水加热至沸腾时,打开盛液体A的分液漏斗开关.左边锥形瓶中水停止沸腾.停止加热后,打开盛液体B的分液漏斗开关,震荡右边锥形瓶.则左边锥形瓶中的水又沸腾.据此推断:锥形瓶中的固体可能是
如图所示,用酒精灯给锥形瓶中的水加热至沸腾时,打开盛液体A的分液漏斗开关.左边锥形瓶中水停止沸腾.停止加热后,打开盛液体B的分液漏斗开关,震荡右边锥形瓶.则左边锥形瓶中的水又沸腾.据此推断:锥形瓶中的固体可能是