题目内容
15.发射火箭所用的燃料液态偏二甲肼(C2H8N2)与N2O4发生的反应可写作:C2H8N2+2N2O4 $\frac{\underline{\;点燃\;}}{\;}$3N2↑+2CO2↑+nH2O,则n等于( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
分析 根据质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断n的数值即可.
解答 解:由题意,火箭所用的燃料液态偏二甲肼(C2H8N2)与N2O4发生的反应可写作:C2H8N2+2N2O4═3N2↑+2CO2↑+nH2O↑,根据反应前后氢原子的数目相等,则8=2n,n=4.
故选:C.
点评 本题难度不大,灵活运用化学反应前后元素守恒、原子守恒是正确解答此类题的关键.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
5.下列各组物质,按单质、化合物、混合物的顺序排列的是( )
| A. | 水银、二氧化碳、液态氧 | B. | 氢气、冰水混合物、加碘食盐 | ||
| C. | 空气、高锰酸钾、石灰水 | D. | 稀有气体、酱油、矿泉水 |
6.节能减排、低碳出行是我们倡导的生活方式,“低碳”指的是尽量减少二氧化碳的排放.下列有关二氧化碳的说法正确的是( )
| A. | 二氧化碳通入紫色石蕊溶液,溶液变为红色,说明二氧化碳具有酸性 | |
| B. | 实验室中可用块状石灰石和稀硫酸反应制取二氧化碳气体 | |
| C. | 二氧化碳和一氧化碳的组成元素相同,在一定条件下可以相互转化 | |
| D. | 进入久未开启的菜窖之前,必须做灯火试验,是因为二氧化碳有毒 |
7.下列有关水的认识中正确的是( )
| A. | 地球水资源丰富,我们没有必要节约用水 | |
| B. | 长期饮用蒸馏水对身体健康没有好处 | |
| C. | 自然界中的水,过滤之后澄清透明,就成了软水 | |
| D. | 工业废水只要无色透明就可以直接饮用 |
7.某反应的微观过程如图,下列说法正确的是( )


| A. | 反应过程中元素的化合价没有发生改变 | |
| B. | 原子种类在化学反应中发生了变化 | |
| C. | 丁分子由两种原子构成,原子个数比是2:1 | |
| D. | 该反应是化合反应 |
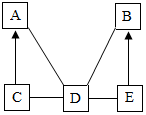 A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质,B在空气中易潮解,C是红棕色固体,E俗称纯碱,图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题:
A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质,B在空气中易潮解,C是红棕色固体,E俗称纯碱,图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题:
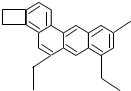 化学家Tim Richard将分子结构坚实像像狗的某有机物(如图所示)取名为“小狗烯”(化学式为C26H26).下列说法正确的是( )
化学家Tim Richard将分子结构坚实像像狗的某有机物(如图所示)取名为“小狗烯”(化学式为C26H26).下列说法正确的是( )