题目内容
14.根据如图提供的仿息,回答相关问题.
(1)图A中铝原子的核电荷数为13,2个铝离子用化学符号表示为2Al3+;
(2)E中X为8,C在化学反应中易失 (填“得”或“失”)电子达到稳定结构.
(3)写出B和D两种微粒组成化合物的化学式MgCl2.
(4)写出一个与D化学性质相似的元素符号F.
分析 (1)根据图中元素周期表可以获得的信息:左上角的数字表示原子序数,原子序数=核电荷数;离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字.
(2)当质子数=核外电子数,为原子,若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子,据此进行分析解答.
(3)B质子数=12,核外电子数=10,质子数>核外电子数,为带2个单位正电荷的镁离子;D质子数=17,核外电子数=18,质子数<核外电子数,为带1个单位负电荷的氯离子;据此进行分析解答.
(4)根据最外层电子数决定元素的化学性质来分析.
解答 解:(1)根据元素周期表中的一格可知,左上角的数字为13,表示原子序数为13;根据原子序数=核电荷数,则图A中铝原子的核电荷数为13.
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故2个铝离子可表示为:2Al3+.
(2)当质子数=核外电子数,为原子,18=2+8+X,X=8.
C的最外层电子数是2,小于4,在化学反应中易失去2个电子而形成阳离子.
(3)B质子数=12,核外电子数=10,质子数>核外电子数,为带2个单位正电荷的镁离子;D质子数=17,核外电子数=18,质子数<核外电子数,为带1个单位负电荷的氯离子;化合价的数值等于离子所带电荷的数值,且符号一致,则镁元素显+2价,氯元素显-1价,形成化合物的化学式为:MgCl2.
(4)D是氯元素,其原子最外层有7个电子,在化学反应中易得到一个电子,氟原子的原子核外也是7个电子,在化学反应中易得到1个电子,二者化学性质相似.
故答案为:(1)13;2Al3+;(2)8;失;(3)MgCl2;(4)F.
点评 本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、粒子结构示意图的含义是正确解答本题的关键.

 阅读快车系列答案
阅读快车系列答案| A. | 碳酸钙-纯 碱 | B. | 氯化钠-食 盐 | C. | 碳酸钠-小苏打 | D. | 氧化钙-熟石灰 |
| A. | 动植物的呼吸 | B. | 酒和醋的酿造 | C. | 食物腐烂 | D. | 水的挥发 |
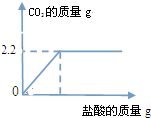 某校兴趣小组为探究石灰石中碳酸钙的质量分数,进行了下列实验:称取6.5g石灰石样品,再加入足量的稀盐酸,充分反应后(杂质不溶于水,也不与稀盐酸反应),产生的CO2和消耗的稀盐酸的质量关系如图所示.求:石灰石中碳酸钙的质量分数.
某校兴趣小组为探究石灰石中碳酸钙的质量分数,进行了下列实验:称取6.5g石灰石样品,再加入足量的稀盐酸,充分反应后(杂质不溶于水,也不与稀盐酸反应),产生的CO2和消耗的稀盐酸的质量关系如图所示.求:石灰石中碳酸钙的质量分数.