题目内容
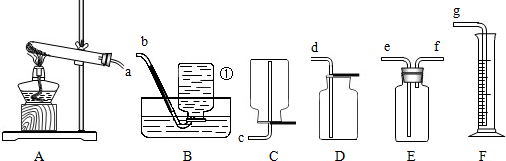
将55克含杂质的干燥氧化铜试样放入试管中,先通氢气后加热,待完全反应后冷却称得残留物45克(杂质不气化、不反应)求:
(1)生成铜多少克?
(2)该氧化铜试样中氧化铜的质量分数?
(1)生成铜多少克?
(2)该氧化铜试样中氧化铜的质量分数?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:由55克到45克,根据氢气还原氧化铜生成铜和水,可知:反应前后固体减少的质量是参加反应的氧化铜中氧元素的质量,利用氢气还原氧化铜的化学方程式,据前后减少的质量差,即氧元素的质量可求出生成的铜的质量,因为物质是完全反应,因此可求出参加反应的氧化铜的质量,进而计算试样中氧化铜的质量分数.
解答:解:设生成的铜的质量是x,试样中氧化铜的质量为y
CuO+H2
Cu+H2O 固体减少的质量
80 64 80-64=16
y x 55g-45g=10g
=
x=40g
=
y=50g
所以氧化铜试样中氧化铜的质量分数是:
×100%≈90.9%
答:(1)生成铜40g;
(2)该氧化铜试样中氧化铜的质量分数是90.9%.
CuO+H2
| ||
80 64 80-64=16
y x 55g-45g=10g
| 64 |
| 16 |
| x |
| 10g |
| 80 |
| 16 |
| y |
| 10g |
所以氧化铜试样中氧化铜的质量分数是:
| 50g |
| 55g |
答:(1)生成铜40g;
(2)该氧化铜试样中氧化铜的质量分数是90.9%.
点评:本题是根据化学反应中物质的质量差来求出反应中其他物质的质量,掌握差量法的应用即可顺利解答.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
田径比赛的发令枪打响时,产生的白烟是( )
| A、二氧化硫 | B、五氧化二磷 |
| C、水 | D、四氧化三铁 |
下列关于燃烧现象的描述中正确的是( )
| A、木炭在空气中燃烧后,生成黑色的固体 |
| B、硫粉在氧气中燃烧,产生微弱的淡蓝色火焰,有刺激性气味的气体生成 |
| C、镁条在空气中燃烧,发出耀眼的白光,有白色的固体生成 |
| D、铁丝在氧气中燃烧,火星四射,有黑色的固体四氧化三铁生成 |
下列变化属于化学变化的是( )
| A、冰棒融化 | B、木材燃烧 |
| C、湿衣服晾干 | D、酒精挥发 |
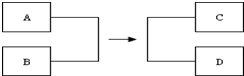 ABCD是初中化学中常见的物质,它们的相互转化关系如图所示
ABCD是初中化学中常见的物质,它们的相互转化关系如图所示
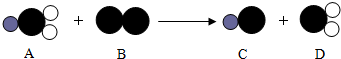
 表示钠原子,
表示钠原子, 表示氯原子,
表示氯原子, 表示氧原子)
表示氧原子)