题目内容
5.实验室测定黄铜的质量分数,取10g样品加入到200g的稀硫酸中恰好完全反应,过滤得到滤液质量为206.3g,则样品中铜的质量分数为( )| A. | 40% | B. | 65% | C. | 47% | D. | 35% |
分析 铜的金属活动性在(H)后,不能与稀硫酸发生反应.利用锌与稀硫酸反应的化学方程式和滤液的增量,列出比例式,就可计算出原混合物中锌的质量.
解答 解:设黄铜中锌的质量为x、
Zn+H2SO4═ZnSO4+H2↑ 滤液增量
65 2 65-2=63
x 206.3g-200g=6.3g
$\frac{65}{x}=\frac{63}{6.3g}$
x=6.5g
样品中铜的质量分数为$\frac{10g-6.5g}{10g}×$100%=35%
答案:D
点评 本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
16.下列一定属于化学变化的是( )
| A. | 氢气燃烧 | B. | 干冰升华 | C. | 滴水成冰 | D. | 石油的分馏 |
13.12g石灰石与足量稀盐酸反应(杂质不与酸反应也不溶于酸),剩余固体的质量与反应时间的关系如表
求:(1)石灰石中碳酸钙的质量分数?
(2)生成二氧化碳的质量.
| 反应时间t/s | t1 | t2 | t3 | t4 |
| 反应后固体的质量m/g | 6 | 4.8 | 2 | 2 |
(2)生成二氧化碳的质量.
20.如图是钠元素和氯元素在元素周期表中的信息和有关的4种粒子结构示意图,下列说法正确的是( )
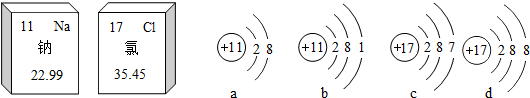
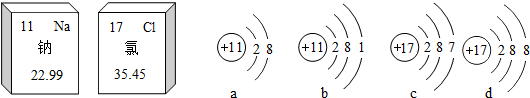
| A. | 钠、氯都属于金属元素 | B. | 氯化钠是由a,d两种粒子构成的 | ||
| C. | 氯的相对原子质量是35.45g | D. | a表示的是一种阴离子 |
17.下列生活用品使用的材料属于有机合成材料的是( )
| A. |  塑料保鲜膜 | B. |  纯棉毛巾 | C. |  真丝围巾 | D. |  不锈钢锅 |
13.欲除去下列物质中的少量杂质(括号内为杂质),所采取的方法错误的是( )
| 选项 | 物质 | 加入的试剂或操作 |
| A | CuO(C) | 在空气中灼烧 |
| B | NaCl(泥沙) | 加足量的水,溶解、过滤、蒸发 |
| C | 稀硫酸(稀盐酸) | 加适量氯化钡溶液,过滤 |
| D | CO2(H2O) | 通过足量的浓硫酸,洗气 |
| A. | A | B. | B | C. | C | D. | D |
12.用如图所示的装置来测定空气中氧气的含量,对该实验认识错误的是( )


| A. | 铜粉用量的多少,不会影响实验结果 | |
| B. | 实验结束后冷却到室温才能读数 | |
| C. | 气球的作用是调节气压,使氧气完全反应 | |
| D. | 在正常操作情况下,反应结束后消耗氧气的总体积将应该是反应前注射器内气体体积和玻璃管中气体总体积的$\frac{1}{5}$ |
 化学新材料的应用,使人们的生活质量不断提高.如图是不同年代常用的水管.
化学新材料的应用,使人们的生活质量不断提高.如图是不同年代常用的水管.