题目内容
完成下列变化的化学方程式,并按要求填空.
(1)二氧化碳转化为一氧化碳的反应:
(2)镁和稀盐酸反应:
(3)高炉内用一氧化碳还原氧化铁:
(4)用纳米级的某种氧化物作催化剂,使汽车尾气中的CO和NO迅速反应转化为两种气体,其中一种是空气中含量最多的气体.请写出该转化的化学方程式:
(1)二氧化碳转化为一氧化碳的反应:
CO2+C
2CO
| ||
CO2+C
2CO
:反应类型是
| ||
化合反应
化合反应
.(2)镁和稀盐酸反应:
Mg+2HCl═MgCl2+H2↑
Mg+2HCl═MgCl2+H2↑
,该反应属于放热
放热
(选填“放热”或“吸热”)反应.(3)高炉内用一氧化碳还原氧化铁:
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
,高炉的产品是
| ||
生铁
生铁
(写物质的名称).(4)用纳米级的某种氧化物作催化剂,使汽车尾气中的CO和NO迅速反应转化为两种气体,其中一种是空气中含量最多的气体.请写出该转化的化学方程式:
2CO+2NO
2CO2+N2
| ||
2CO+2NO
2CO2+N2
.
| ||
分析:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答:解:(1)二氧化碳在高温下与碳反应生成一氧化碳,反应的化学方程式为:CO2+C
2CO;该反应符合“多变一”的特征,属于化合反应.
(2)镁和稀盐酸反应生成氯化镁和氢气,反应的化学方程式为:Mg+2HCl═MgCl2+H2↑;该反应放出大量的热.
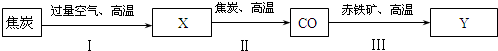
(3)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO
2Fe+3CO2.高炉的产品是生铁.
(4)汽车尾气中的CO跟NO反应转化成两种气体,其中一种可参与植物的光合作用(二氧化碳),另一种是空气中含量最多的气体(氮气),反应的化学方程式为2CO+2NO
2CO2+N2.
故答案为:(1)CO2+C
2CO;化合反应;(2)Mg+2HCl═MgCl2+H2↑;放热;(3)Fe2O3+3CO
2Fe+3CO2;生铁;(4)2CO+2NO
2CO2+N2.
| ||
(2)镁和稀盐酸反应生成氯化镁和氢气,反应的化学方程式为:Mg+2HCl═MgCl2+H2↑;该反应放出大量的热.
(3)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO
| ||
(4)汽车尾气中的CO跟NO反应转化成两种气体,其中一种可参与植物的光合作用(二氧化碳),另一种是空气中含量最多的气体(氮气),反应的化学方程式为2CO+2NO
| ||
故答案为:(1)CO2+C
| ||
| ||
| ||
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目