题目内容
小敏对实验室用石灰石和稀盐酸制取二氧化碳后的废液,进行溶质成分鉴定.取废液上层清液50克,逐滴加入质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克开始出现白色沉淀.继续滴加至沉淀不再产生,过滤,测得沉淀的质量为5克,并绘制了图象.

(1)滴加的溶液中溶质属于_____(填“盐”或“碱”).
(2)10克碳酸钠溶液中含有的溶质质量是______克.
(3)图中a点的数值是____________.
(4)废液中含有的溶质是________(写化学式).
(5)通过计算说明,图象横坐标中的b点表示的溶液的质量是多少克?(书写过程)________
盐 2.65 1.1 HCl CaCl2 30g 【解析】试题分析:1)滴加的碳酸钠属于盐类。 2)10g碳酸钠溶液中含溶质的质量为:10g╳26.5%=2.65g 3)图中a点表示生成气体的最大值。可利用二氧化碳与碳酸钠在反应中的质量关系进行求解。解题过程为: 【解析】 设生成二氧化碳气体的质量为x 2HCl+Na2CO3= 2NaCl+H2O+CO2↑ 1...除去下列物质中混有的少量杂质,所用方法不正确的是( )
选项 | 物质 | 杂质 | 除去杂质的方法 |
A | NaCl | 泥沙 | 加入水溶解,过滤,蒸发 |
B | O2 | 水蒸气 | 通过足量的浓硫酸 |
C | NaOH溶液 | Na2CO3溶液 | 滴入足量的稀盐酸至不再产生气体 |
D | H2 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
A. A B. B C. C D. D
C 【解析】除去杂质的原则是所选试剂只与杂质反应,且不引入新的杂质。A、氯化钠易溶于水,泥沙难溶于水,加入水溶解,过滤,蒸发可得到氯化钠,正确;B、浓硫酸具有吸水性,可除去氧气中的水蒸气,正确;C、Na2CO3+2HCl==2NaCl+H2O+CO2↑,引入杂质氯化钠,错误;D、先通过NaOH溶液,可除去HCl气体,再通过浓硫酸除去引入的水蒸气,得到干燥、纯净的氢气,正确。故选C。实验与探究是化学学习的重要方法和内容,李明看到家里多年未用的铜制火锅上有绿色的锈迹,他对绿色锈迹的成分和性质产生了浓厚兴趣。
【查阅资料】
(1)碱石灰是CaO和NaOH的固体混合物;(2)铜表面绿色锈迹的主要成分为碱式酸铜。
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成。为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体成分。
【猜想与假设】该黑色固体可能是①碳粉;②氧化铜;③_______________________________。
【设计方案】请帮助该同学完成下述实验报告:
实验操作与现象 | 实验结论 |
___________________ | 猜想②正确 |
探究二:碱式碳酸铜受热分解还会生成CO2和H2O。
【进行实验】选择如下图所示装置进行验证
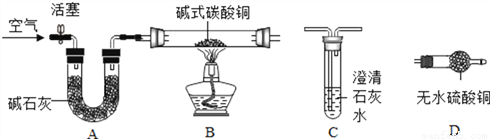
步骤一:连接A和B,打开活塞,通入一段时间的空气;
步骤二:点燃酒酒精灯,依次连接装置A→B→________→_______(填“C”,“D”);
步骤三:点燃酒精灯,观察到明显现象后,停止加热。
【解释与结论】
①当观察到_________________________________,说明碱式碳酸铜受热分解生成了H2O,写出装置C中反应的化学方程式________________________;
②写出Cu2(OH)2CO3受热分解的化学方程式___________________;
【反思与评价】
上述装置中A的作用是________________________。
炭粉和氧化铜 取少量样品于试管中,加入足量稀硫酸,若固体全部溶解,溶液变为蓝色 D C D中固体变蓝 CO2+Ca(OH)2=CaCO3↓+H2O Cu2(OH)2CO3=2CuO+H2O+CO2 ↑ 除尽空气中的二氧化碳和水 【解析】(1)该黑色固体可能是碳粉盒氧化铜的混合物; (2)氧化铜可以与酸反应生成蓝色的溶液,而碳不与酸反应,故可以取少量样品于试管中,加入足量稀硫酸,若固体全...


 ”和“
”和“ ”表示两种不同的原子,据图分析下列说法正确的是( )
”表示两种不同的原子,据图分析下列说法正确的是( )
 2H2O
2H2O