题目内容
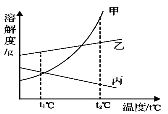
下图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线。现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在)。下列说法正确的是
A.三种物质溶解度大小依次为:乙>丙>甲
B.将温度由t2℃降到t1℃时,析出甲的质量比乙多
C.若甲中含有少量杂质乙,可采用降温结晶的方法进行提纯
D.将温度由t2℃降到t1℃,所得溶液中溶质的质量分数由大到小的顺序为:乙>丙=甲
C
【解析】
试题分析:A、要比较不同物质溶解度的大小关系,一定要指明温度,错误,B、根据曲线,甲物质的溶解度随温度的变化比乙物质要大,故将等质量的饱和溶液,温度由t2℃降到t1℃时,析出甲的质量比乙多,而没有说明是否是等质量,所以无法比较,错误,C、根据曲线,甲物质的溶解度随温度温度的升高而增大,故若甲中含有少量杂质乙,可采用降温结晶的方法进行提纯,正确,D、根据曲线,甲、乙两物质的溶解度都随温度的升高而增大,将温度由t2℃降到t1℃,都有溶质析出,成为t1℃的饱和溶液,此时乙的溶解度大于甲,故溶液中溶质的质量分数乙>甲,而丙物质的溶解度随温度的升高而降低,故将丙物质的饱和溶液由t2℃降到t1℃,由饱和溶液变为不饱和溶液,溶液的溶质质量分数不变,仍然跟在t2℃时的溶质质量分数一样,从溶解度曲线看出,甲在t1℃的溶解度要大于丙在t2℃的溶解度,故溶质质量分数甲要大于丙,故所得溶液中溶质的质量分数由大到小的顺序为:乙>甲>丙,错误,故选C
考点:溶解度曲线的意义,饱和、不饱和溶液的转化,结晶的方法,溶质质量分数的计算

(4分)酸、碱、盐溶解性表是学习化学的重要工具。下表列出了部分酸、碱、盐在20℃时的溶解性。利用此表完成下列各小题:
离子 | OH- | Cl- | SO42- |
H+ | 溶、挥 | 溶 | |
Na+ | 溶 | 溶 | 溶 |
Ca2+ | 微 | 溶 | 微 |
Cu2+ | 不 | 溶 | 溶 |
(1)查:CaSO4的溶解性 ;
(2)写出表中空格处物质的化学式 ;
(3)运用此表,写出一个生成蓝色溶液且属于中和反应的化学方程式: 。
某石灰厂有一批石灰石原料,为了测定该石灰石的纯度,厂化验 室技术员称取6.25 g研碎的石灰石粉末,进行四次高温煅烧(杂质没有变化)、冷却、称量剩余固体质量的重复操作,记录数据如下:(提示:碳酸钙在高温下分解,生成氧化钙和二氧化碳气体)
室技术员称取6.25 g研碎的石灰石粉末,进行四次高温煅烧(杂质没有变化)、冷却、称量剩余固体质量的重复操作,记录数据如下:(提示:碳酸钙在高温下分解,生成氧化钙和二氧化碳气体)
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量 | 5.55g | 4.35g | 4.05g | 4.05g |
试计算:
(1)完全反应后生成二氧化碳 g;
(2)石灰石样品中碳酸钙的质量分数(计算结果精确到0.1%)。

 B.
B. C.
C. D.
D.
