题目内容
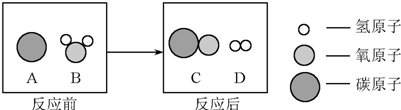
 有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应有CO2气体产生,D与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀.
有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应有CO2气体产生,D与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀.(1)请根据已知条件推断四种物质的化学式:
A
(2)请写出下列反应的化学方程式:
C溶液中通入CO2,溶液变浑浊
考点:物质的鉴别、推断,化学式的书写及意义,书写化学方程式、文字表达式、电离方程式
专题:框图型推断题
分析:根据题目中的信息和图框可知:C和二氧化碳反应溶液变浑浊且生成白色沉淀A,A为盐,A高温分解生成B,D和A反应有二氧化碳产生,A是盐,则D是酸,D和硝酸银反应生成不溶于稀硝酸的白色沉淀,则D是HCl,C和D发生中和反应,则C是碱,B和水反应生成C,则B是碱性氧化物,A高温分解生成碱性氧化物,则A是CaCO3,B是CaO,C是Ca(OH)2.代入检验,是否符合题意.
解答:解:
根据题目中的信息和图框可知:CC和二氧化碳反应溶液变浑浊且生成白色沉淀A,A为盐,A高温分解生成B,D和A反应有二氧化碳产生,A是盐,则D是酸,D和硝酸银反应生成不溶于稀硝酸的白色沉淀,则D是HCl,C和D发生中和反应,则C是碱,B和水反应生成C,则B是碱性氧化物,A高温分解生成碱性氧化物,则A是CaCO3,B是CaO,C是Ca(OH)2.代入检验,符合题意.
(1)通过以上分析知,A、B、C、D分别是CaCO3、CaO、Ca(OH)2、HCl,
(2)二氧化碳和氢氧化钙反应生成碳酸钙和水,反应方程式为:Ca(OH)2+CO2═CaCO3↓+H2O,
D与C的反应是氢氧化钙和盐酸反应生成氯化钙和水,化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O
故答案为:
(1)CaCO3;CaO;Ca(OH)2;HCl;
(2)Ca(OH)2+CO2═CaCO3↓+H2O;Ca(OH)2+2HCl=CaCl2+2H2O
根据题目中的信息和图框可知:CC和二氧化碳反应溶液变浑浊且生成白色沉淀A,A为盐,A高温分解生成B,D和A反应有二氧化碳产生,A是盐,则D是酸,D和硝酸银反应生成不溶于稀硝酸的白色沉淀,则D是HCl,C和D发生中和反应,则C是碱,B和水反应生成C,则B是碱性氧化物,A高温分解生成碱性氧化物,则A是CaCO3,B是CaO,C是Ca(OH)2.代入检验,符合题意.
(1)通过以上分析知,A、B、C、D分别是CaCO3、CaO、Ca(OH)2、HCl,
(2)二氧化碳和氢氧化钙反应生成碳酸钙和水,反应方程式为:Ca(OH)2+CO2═CaCO3↓+H2O,
D与C的反应是氢氧化钙和盐酸反应生成氯化钙和水,化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O
故答案为:
(1)CaCO3;CaO;Ca(OH)2;HCl;
(2)Ca(OH)2+CO2═CaCO3↓+H2O;Ca(OH)2+2HCl=CaCl2+2H2O
点评:本题考查了无机物的推断,明确物质的性质及物质间的转化是解本题关键,注意能和二氧化碳反应生成白色沉淀的离子不仅有钙离子,含有镁离子、钡离子等.

练习册系列答案
相关题目
下列物质中,随着温度的升高,在水中的溶解度减小的是( )
| A、熟石灰 | B、食盐 |
| C、硝酸钾 | D、氯化铵 |