题目内容
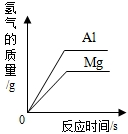
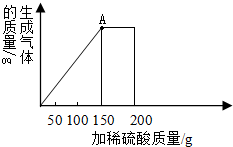
为测定铜锌合金的组成,某化学小组的同学将200克稀硫酸分四次加入到40克合金中,得出如下数据和图象.
请计算:
(1)a的数值为______.
(2)合金中铜的质量分数为______.
(3)实验所用稀硫酸的质量分数是______.
| 次数 | 第1次 | 第2次 | 第3次 |
| 加入稀硫酸的质量/g | 50 | 50 | 50 |
| 剩余固体的质量/g | 33.5 | a | 20.5 |
(1)a的数值为______.
(2)合金中铜的质量分数为______.
(3)实验所用稀硫酸的质量分数是______.

(1)有图象可以看出在加入到150g时酸与金属恰好完全反应,有表格可以看出每消耗50g硫酸反应的锌的质量是6.5g,所以a=40g-6.5g×2=27
故答案为:27
(2)最后剩余的金属是铜,质量是20.5g,合金中铜的质量分数为
×100%=51.3%.
故答案为:51.3%
(3)设硫酸的溶质质量分数是x
Zn+H2SO4=ZnSO4+H2↑
65 98
6.5g 50g×x
=
x=19.6%
故答案为:19.6%
故答案为:27
(2)最后剩余的金属是铜,质量是20.5g,合金中铜的质量分数为
| 20.5g |
| 40g |
故答案为:51.3%
(3)设硫酸的溶质质量分数是x
Zn+H2SO4=ZnSO4+H2↑
65 98
6.5g 50g×x
| 65 |
| 98 |
| 6.5g |
| 50g×x |
x=19.6%
故答案为:19.6%

练习册系列答案
相关题目