题目内容
久置于空气中的氢氧化钠变质,生成碳酸钠,其检验方法是取样品少量置于试管中,加入 可证明NaOH已变质.用化学方程式表示变质原因和检验原理 , ,若除去已变质的Na2CO3,应进行下列操作:先溶解,再加入适量的 试剂,过滤、蒸发,起反应的化学方程式是 .
考点:碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水,写出反应的化学方程式即可;检验氢氧化钠变质的产物含碳酸钠,碳酸盐能与酸反应生成能使澄清石灰水变浑浊的二氧化碳气体,检验碳酸盐最简单的方法是滴加盐酸;碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠.
解答:解:氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O.
碳酸盐中含有碳酸根离子,碳酸根离子的检验方法是:将该碳酸盐少许于试管中,加入少量稀盐酸,观察到有气泡产生;将产生的气体通入澄清石灰水中,澄清石灰水变浑浊,说明该物质中含有碳酸根离子,说明该物质是碳酸盐.故检验氢氧化钠变质的产物含碳酸钠,再滴入足量的稀盐酸,有气泡产生;碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
碳酸钠溶液与适量的氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠溶液,充分反应后应过滤、蒸发,可除去Na2CO3.方程式为Na2CO2+Ca(OH)2=2NaOH+CaCO3↓
故答案为:稀盐酸;2NaOH+CO2=Na2CO3+H2O;Na2CO3+2HCl═2NaCl+H2O+CO2↑;澄清的石灰水;Na2CO2+Ca(OH)2=2NaOH+CaCO3↓.
碳酸盐中含有碳酸根离子,碳酸根离子的检验方法是:将该碳酸盐少许于试管中,加入少量稀盐酸,观察到有气泡产生;将产生的气体通入澄清石灰水中,澄清石灰水变浑浊,说明该物质中含有碳酸根离子,说明该物质是碳酸盐.故检验氢氧化钠变质的产物含碳酸钠,再滴入足量的稀盐酸,有气泡产生;碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
碳酸钠溶液与适量的氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠溶液,充分反应后应过滤、蒸发,可除去Na2CO3.方程式为Na2CO2+Ca(OH)2=2NaOH+CaCO3↓
故答案为:稀盐酸;2NaOH+CO2=Na2CO3+H2O;Na2CO3+2HCl═2NaCl+H2O+CO2↑;澄清的石灰水;Na2CO2+Ca(OH)2=2NaOH+CaCO3↓.
点评:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
将10克溶质质量分数为36%的浓盐酸稀释成15%的稀盐酸,需加水的质量为( )
| A、11克 | B、13克 |
| C、14克 | D、16 克 |
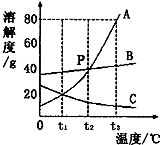 如图是 A、B、C三种物质的溶解度曲线,回答下列问题:
如图是 A、B、C三种物质的溶解度曲线,回答下列问题: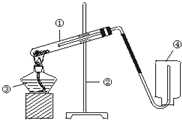 如图是实验室用加热高锰酸钾的方法制取氧气的装置图,请回答下列几个问题:
如图是实验室用加热高锰酸钾的方法制取氧气的装置图,请回答下列几个问题: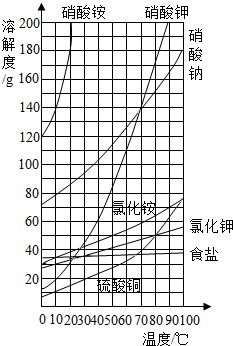 据图中几种物质的溶解度曲线,回答下列问题:
据图中几种物质的溶解度曲线,回答下列问题: ”和“
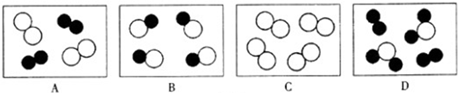
”和“ ”表示不同元素的原子,其中表示化合物的是
”表示不同元素的原子,其中表示化合物的是