题目内容
溶液在我们日常生活中有很广泛的用途,下列属于溶液的是( )
A .蒸馏水 B .碘酒 C .石灰浆 D .植物油
B

 名校课堂系列答案
名校课堂系列答案下表是KCl固体在不同温度时的溶解度。下列说法错误的是
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 |
A.KCl固体的溶解度随温度的升高而增大 B.80℃时,KCl固体的溶解度是51.1g
C.60℃的KCl饱和溶液降温后会有晶体析出 D.20℃时,KCl饱和溶液的溶质质量分数为34.0%
某化学小组初步探究“氢氧化钠溶液与盐酸发生中和反应时溶液温度的变化情况”。
实验用品:37%的浓盐酸(密度为1.18g/mL)、10%的氢氧化钠溶液、蒸 馏水、量筒、温
馏水、量筒、温 度计
度计
实验一:配制100mL10%的盐酸(密度为1.05g/mL)
实验步骤
(1)计算:需要37%的浓盐酸的体积为 mL(精确到0.01mL,下同);需要蒸馏水的体积为 mL(水的密度为1.0g/mL)
(2)量取浓盐酸和蒸馏水。
(3)混合配制。
实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:
| 加入盐酸的体积(V)/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 溶液温度变化(△t)/℃ | △t1 | 5.2 | 9.6 | 12.0 | 16.0 | 18.2 | 16.7 | 15.7 | 14.7 | 13.7 | 12.9 |
(1)表中△t1的值为 。
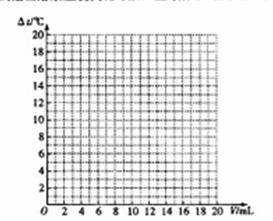 (2)试绘出溶液温度变化与加入盐酸体积之间的关系图。
(2)试绘出溶液温度变化与加入盐酸体积之间的关系图。
(3)根据所绘曲线分析,加入盐酸的体积在0~10mL时,溶液温度变化的趋势及其原因是
。
(4)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素)。
横坐标及猜想理由: ;
纵坐标及猜想理由: 。
 2NaH可实现氢气的存储,计算230g金属钠最多可吸收氢气的质量.
2NaH可实现氢气的存储,计算230g金属钠最多可吸收氢气的质量.
 。
。 mL气体,则负极产生气体的体积是 mL,该实验证明了水是由 组成的。
mL气体,则负极产生气体的体积是 mL,该实验证明了水是由 组成的。 ②生活中常用 来降低水的硬度。右图是常用自制净水器,其中活性炭的作用是 ;制造塑料瓶的材料属于 材料。请介绍一种你的节水方法 合理均可)。
②生活中常用 来降低水的硬度。右图是常用自制净水器,其中活性炭的作用是 ;制造塑料瓶的材料属于 材料。请介绍一种你的节水方法 合理均可)。