题目内容
乙醇(C2H5OH)俗称酒精,可通过粮食发酵等方法得到,燃烧时放出大量的热量,其燃烧反应方程式是C2H5OH+3O2 2CO2+3H2O,试计算.
2CO2+3H2O,试计算.(1)一个乙醇分子里含有______个原子
(2)乙醇中碳元素的质量分数为______.
(3)4.6克乙醇完全燃烧能生成多少克二氧化碳?(写出计算过程)
【答案】分析:(1)根据乙醇的化学式计算一个乙醇分子里含有的原子数;
(2)根据乙醇的化学式计算乙醇中碳元素的质量分数为;
(3)根据乙醇燃烧的反应,由乙醇的质量可求出生成二氧化碳的质量.
解答:解:(1)一个乙醇分子里含有的原子数是:2+5+1+1=9;
(2)乙醇中碳元素的质量分数为: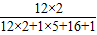 ×100%=52.2%
×100%=52.2%
(3)设:4.6克乙醇完全燃烧能生成二氧化碳的质量为x
C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
46 2×44
4.6 g x
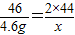 解得:x=
解得:x=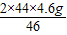 =8.8 g
=8.8 g
故答为:(1)9;(2)52.2%;(3)4.6克乙醇完全燃烧能生成二氧化碳的质量为8.8克.
点评:本题较为简单,理解化学式的意义、正确书写乙醇燃烧的方程式是计算的基础.
(2)根据乙醇的化学式计算乙醇中碳元素的质量分数为;
(3)根据乙醇燃烧的反应,由乙醇的质量可求出生成二氧化碳的质量.
解答:解:(1)一个乙醇分子里含有的原子数是:2+5+1+1=9;
(2)乙醇中碳元素的质量分数为:
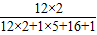 ×100%=52.2%
×100%=52.2%(3)设:4.6克乙醇完全燃烧能生成二氧化碳的质量为x
C2H5OH+3O2
 2CO2+3H2O
2CO2+3H2O 46 2×44
4.6 g x
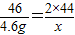 解得:x=
解得:x=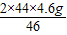 =8.8 g
=8.8 g 故答为:(1)9;(2)52.2%;(3)4.6克乙醇完全燃烧能生成二氧化碳的质量为8.8克.
点评:本题较为简单,理解化学式的意义、正确书写乙醇燃烧的方程式是计算的基础.

练习册系列答案
相关题目
随着经济的发展,能源与环境成为人们日益关注的问题.
(1)减少煤、 和天然气等化石燃料的燃烧,会有助于减少二氧化碳的产生.
(2)化石燃料的特点是 (填字母序号).
A.不可再生 B.清洁燃料 C.资源有限 D.新型能源
(3)目前,人们正在利用和开发新能源,如太阳能、核能、地热能、 能等.
(4)我市家庭厨房中的“柴”多数使用天然气,它的主要成分的名称是 ,燃烧的化学方程式是 .
(5)在密闭容器中,将少量乙醇(C2H5OH)置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质W.现测得反应前后各物质的质量如下:
①根据质量守恒定律,得出表中x的值为 ;
②根据表中数据,可确定未知物W中所含元素及各组成元素的质量为 .
(1)减少煤、
(2)化石燃料的特点是
A.不可再生 B.清洁燃料 C.资源有限 D.新型能源
(3)目前,人们正在利用和开发新能源,如太阳能、核能、地热能、
(4)我市家庭厨房中的“柴”多数使用天然气,它的主要成分的名称是
(5)在密闭容器中,将少量乙醇(C2H5OH)置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质W.现测得反应前后各物质的质量如下:
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水蒸气 | W |
| 反应前的质量/g | 46 | 88 | 0 | 0 | 0 |
| 反应后的质量/g | 0 | 8 | 44 | 54 | x |
②根据表中数据,可确定未知物W中所含元素及各组成元素的质量为