题目内容
13.将一定量的苯(C6H6)和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水和一种未知物X.测得反应前后物质的质量如下表:| 物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 1.3 | 3.2 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 2.2 | 0.9 | m |
| A. | 表中m的值为4.5 | B. | 该反应属于分解反应 | ||
| C. | X能在氧气中燃烧 | D. | X中一定含有氢元素 |
分析 根据质量守恒定律可知:反应后质量减少的物质是反应物,质量增加的物质是生成物;根据质量守恒定律可以确定X的质量;通过计算苯、氧气、二氧化碳、水中各元素的质量,推算出X中所含元素的种类.
解答 解:由表格信息可知反应后CO2质量增加了2.2g,是生成物;H2O质量增加了0.9g,是生成物;O2质量减少了3.2g,是反应物;苯的质量减少了1.3g克,是反应物;生成物还少1.4g,所以X是生成物.
A、反应后生成的物质x的质量1.4g,故m的值为1.4,故选项错误.
B、反应物是苯和O2,生成物是CO2、H2O和X,不是分解反应,故选项错误.
C、根据反应前后元素质量相等,苯中含碳元素的质量为$1.3g×\frac{72}{78}×100%$=1.2g,二氧化碳中含有碳元素的质量为2.2g×$\frac{12}{44}×100%$=0.6g,物质X含有碳元素的质量为1.2g-0.6g=0.6g.苯中含氢元素的质量为1.3g×$\frac{6}{78}$=0.1g,2.7g水中含氢元素的质量为0.9g×$\frac{2}{18}$=0.1g,反应前后氢元素的质量相等,故物质X不含有氢元素.则X中含氧元素的质量为:1.4g-1.80.6g=0.8g;X中含有C、O两种元素,两种元素的质量比为0.6g:0.8g=3:4,该物质为CO,具有可燃性,能在氧气中燃烧.故选项正确.
D、由C中计算过程可知:X中含有C、O两种元素,故选项错误.
故选C.
点评 本题难度不是很大,解答本题要认真分析各物质的质量变化情况,仔细推敲,即可求解.

练习册系列答案
相关题目
4.临近中考,小明将学过的化学知识整理如下.你认为完全正确的一组是( )
| A.除杂(括号内为杂质) | B.鉴别 |
| MnO2(KCl)-用水溶解、过滤、干燥 NaCl(Na2CO3)-加适量盐酸后蒸发 KNO3(NaCl)-降温结晶后过滤 | 磷肥和钾肥-观察颜色 羊毛和涤纶-点燃后嗅闻气味 硬水和软水-用肥皂水 |
| C.检验 | D.干燥 |
| 氧气-用带火星的木条检验 二氧化碳-用点燃的木条检验 盐酸-用pH试纸检验 | 氨气-用氢氧化钠固体干燥 二氧化碳-用生石灰干燥 氢气-用浓硫酸干燥 |
| A. | A | B. | B | C. | C | D. | D |
1.分析下列实验操作正确的是( )
| A. | 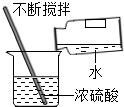 稀释浓硫酸 | B. |  称量氢氧化钠固体 | ||
| C. | 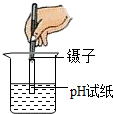 测定溶液的pH | D. | 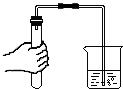 检查装置的气密性 |
8.小明家有包开启了的发酵办粉(小苏打:NaHCO3),久置在灶台上方,可能因受热而变质.小明为此开展了探究,请分析其过程并完成相关内容.
【查阅资料】①2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O
②NaHCO3+NaOH═Na2CO3+H2O
③2NaHCO3+Ca(OH)2═CaCO3↓+Na2CO3+2H2O
④Ca(HCO3)2+Na2CO3═CaCO3↓+2NaHCO3
⑤Na2CO3受热不分解,NaHCO3、Ca(HCO3)2都能溶与水.
【假设猜想】假设一:小苏打没有变质,化学成分为 NaHCO3;
假设二:小苏打完全变质,化学成分为Na2CO3;
假设三:小苏打部分变质NaHCO3和Na2CO3.
【实验方案】可选药品:①Ca(OH)2溶液 ②CaCl2溶液 ③NaOH溶液 ④稀盐酸
【问题讨论】有同学认为,取一定量样品直接加热,再将产生的气体通入澄清石灰水,根据实验现象,对上述三种假设的每一种是否成立都能进行判断.请评价这种方案是否合理及理由:否;不能判断是部分还是没有变质的情况.
【查阅资料】①2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O
②NaHCO3+NaOH═Na2CO3+H2O
③2NaHCO3+Ca(OH)2═CaCO3↓+Na2CO3+2H2O
④Ca(HCO3)2+Na2CO3═CaCO3↓+2NaHCO3
⑤Na2CO3受热不分解,NaHCO3、Ca(HCO3)2都能溶与水.
【假设猜想】假设一:小苏打没有变质,化学成分为 NaHCO3;
假设二:小苏打完全变质,化学成分为Na2CO3;
假设三:小苏打部分变质NaHCO3和Na2CO3.
【实验方案】可选药品:①Ca(OH)2溶液 ②CaCl2溶液 ③NaOH溶液 ④稀盐酸
| 实验操作 | 实验现象 | 实验结论 |
| 操作一:取小苏打样品少量溶于足量水后,加入过量的②(填药品编号,下同),观察,如有沉淀,则继续进行下一步操作. 操作二:待操作一中反应充分后过滤,并在滤液中加入过量的④观察. | 操作一中无沉淀出现[] | 假设一成立 |
| 操作一中有沉淀出现 | 假设二成立 | |
| 操作二中产生气泡 | 假设三成立 |
2.某同学测定硫酸铜晶体(CuSO4•5H2O)里结晶水的含量,请回答下列问题:
(1)实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量.现有坩埚、坩埚钳、三脚架、泥三角、研钵、玻璃棒、干燥器、药匙、酒精灯、火柴、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是托盘天平.实验步骤⑥的目的是使硫酸铜晶体中的结晶水完全失去.
(2)细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,那分解的产物是什么呢?
查阅资料发现:硫酸铜受热分解生成氧化铜和气体,气体是由SO2、SO3、O2中的一种或几种;SO2、SO3都能被碱石灰(氢氧化钠和氧化钙混合物)吸收,SO2、SO3都能被氢氧化钠溶液吸收.同学利用如图装置探究硫酸铜受热分解生成的气体的成分(假设加热硫酸铜粉末直至完全分解).实验结果发现:用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有O2.已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:
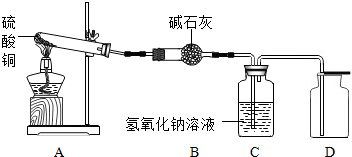
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是哪一个?B
A.3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑ B.4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO3↑+2SO2↑+O2↑
C.5CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+SO3↑+4SO2↑+2O2↑ D.6CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$6CuO+4SO3↑+2SO2↑+O2↑
(1)实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量.现有坩埚、坩埚钳、三脚架、泥三角、研钵、玻璃棒、干燥器、药匙、酒精灯、火柴、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是托盘天平.实验步骤⑥的目的是使硫酸铜晶体中的结晶水完全失去.
(2)细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,那分解的产物是什么呢?
查阅资料发现:硫酸铜受热分解生成氧化铜和气体,气体是由SO2、SO3、O2中的一种或几种;SO2、SO3都能被碱石灰(氢氧化钠和氧化钙混合物)吸收,SO2、SO3都能被氢氧化钠溶液吸收.同学利用如图装置探究硫酸铜受热分解生成的气体的成分(假设加热硫酸铜粉末直至完全分解).实验结果发现:用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有O2.已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:

| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0克 | 75.0克 | 140.0克 |
| 反应后 | 37.0克 | 79.5克 | 140.0克 |
A.3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑ B.4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO3↑+2SO2↑+O2↑
C.5CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+SO3↑+4SO2↑+2O2↑ D.6CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$6CuO+4SO3↑+2SO2↑+O2↑
20.下列做法中,你认为不利于改善我市空气质量的是( )
| A. | 就地焚烧植物的秸杆和垃圾 | B. | 植树种花,搞好绿化 | ||
| C. | 使用清洁能源 | D. | 安装机动车辆尾气净化装置 |