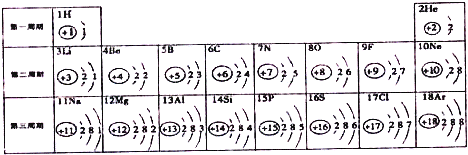
��Ŀ����
��һ���ܱ������з���M��N��Q��P�������ʣ���һ�������·�����ѧ��Ӧ��һ��ʱ�����й��������������ڴ˷�Ӧ��ʶ��ȷ���ǣ�������
| ���� | M | N | Q | P |
| ��Ӧǰ������g�� | 18 | 1 | 2 | 32 |
| ��Ӧ��������g�� | X | 26 | 2 | 12 |
| �� | A�� | ��Ӧ������M������Ϊ23g | B�� | �ñ仯�Ļ�����Ӧ�����ǷֽⷴӦ |
| �� | C�� | ����Q�Ǹ÷�Ӧ�Ĵ��� | D�� | ��Ӧ��N��P��������Ϊ5��4 |
| �����غ㶨�ɼ���Ӧ�ã���Ӧ���͵��ж���. | |||||||||||||||||||||
| ר�⣺ | ��ѧ����������غ㶨�ɣ� | ||||||||||||||||||||
| ������ | ���������غ㶨�ɼ����X��ֵ���ٸ��ݻ�ѧ��Ӧ���������ӵ�������������������ٵ������Ƿ�Ӧ���ϱ������ݽ��з����� | ||||||||||||||||||||
| ��� | �⣺���������غ㶨�ɣ���Ӧǰ�����ʵ����������䣬����18+1+2+32=X+26+2+12�����x=13g��M��P���������٣��Ƿ�Ӧ�N���ӣ��������M��Ӧ����18g��13g=5g��P�ķ�Ӧ����Ϊ32g��12g=20g�����ɵ�N������Ϊ26g��1g=25g�����ݿ������´�����
A����Ӧ������M������xΪ��18g��5g=13g����������ȷ�� B���÷�Ӧ�ķ�Ӧ��Ϊ��M��P��������ΪN�����ϡ����һ�����ص㣬���ڻ��Ϸ�Ӧ�� C������Q�������ڷ�Ӧǰ�䣬�����Ǹ÷�Ӧ�Ĵ�������˵����ȷ�� D����Ӧ��N��P��������Ϊ��25g��20g=5��4����˵����ȷ�� ��ѡ��D�� | ||||||||||||||||||||
| ������ | �ڻ�ѧ��Ӧ����ѭ�����غ㶨�ɣ��μӷ�Ӧ�����ʵ������ܺ͵��ڷ�Ӧ�����ɵ����ʵ������ܺͣ� |

�ӷ��ӵĽǶȷ��������н��Ͳ���ȷ���ǣ�������
| �� | A�� | ˮ�����������ˮ���������� |
| �� | B�� | ������ѹ�������ڸ�ƿ�Щ������Ӽ��м�� |
| �� | C�� | ˮͨ�������������������������ڻ�ѧ�仯�пɷ� |
| �� | D�� | ʪ�·���̫���¸ɵÿ쩁�������˶��������¶��й� |
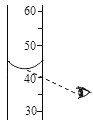
ijѧ����ȡҺ�壬������Һ�尼Һ�����ʹ�����ˮƽ������Ϊ30mL����Һ�嵹��һ���ֺ��Ӷ���Ϊ20mL�����ͬѧʵ�ʵ�����Һ�����Ϊ��������
| �� | A�� | ����10 mL | B�� | С��10 mL | C�� | ����10 mL | D�� | ��ȷ�� |
������ʾ�������뻯ѧ�йص��ǣ�������
�ٽ������ ��������Ʒ ��Һ������ ��ҽҩҩƷ��
| �� | A�� | �٢� | B�� | �ڢ� | C�� | �٢ڢۢ� | D�� | �� |
��ȥ���������л��е�������������Ϊ���ʣ������÷�����ȷ����
ѡ�� | ���� | �������� |
A�� | NaCl��Na2CO3�� | �����������ᡢ�������ᾧ |
B�� | KNO3��Һ��CaCl2�� | �μ�K2CO3��Һ��ǡ����ȫ��Ӧ������ |
C�� | CO2��HCl�� | ͨ��ʢ����������������Һ��ϴ��ƿ |
D�� | Cu��CuO�� | ͨ���������������� |
����ʵ�������ȷ���ǣ�������
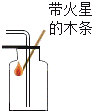
| �� | A�� |
�������� | B�� |
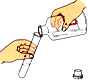
�㵹Һ�� | C�� |
��ȡҺ����� | D�� |
��ȼ�ƾ��� |