题目内容
A、B、C、D、E、F、G为初中化学常见物质,他们之间有如图1所示的反应关系(“→”表示能转化),其中A~E含有一种相同元素,且A是一直单质,F是最常用的灭火剂

(1)写出A物质的一点用途
(2)反应③和反应④的最主要区别是
(3)反应⑧的化学方程式为
(4)反应⑥的化学方程式为
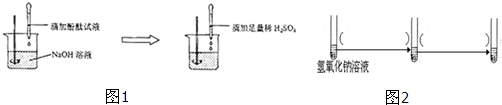
(5)①~⑨中,利用图2所示装置进行试验,能观察到试管中有明显现象有 (填序号),能观察到的现象的是 .

(1)写出A物质的一点用途
(2)反应③和反应④的最主要区别是
(3)反应⑧的化学方程式为
(4)反应⑥的化学方程式为
(5)①~⑨中,利用图2所示装置进行试验,能观察到试管中有明显现象有
考点:物质的鉴别、推断,书写化学方程式、文字表达式、电离方程式
专题:框图型推断题
分析:根据A、B、C、D、E、F、G为初中化学常见物质,F是最常用的灭火剂,所以F可能是水,F会转化成G,G会转化成E,E会转化成F,所以猜想G是氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,所以E是碳酸钙,A~E含有一种相同元素,且A是一种单质,A会转化成B、D,所以A可能是碳,C会转化成D、B、水,D会转化成碳酸钙,所以D是二氧化碳,B就是一氧化碳,所以C可能是甲烷,然后将推出的各种物质进行验证即可.
解答:解:(1)A、B、C、D、E、F、G为初中化学常见物质,F是最常用的灭火剂,所以F可能是水,F会转化成G,G会转化成E,E会转化成F,所以猜想G是氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,所以E是碳酸钙,A~E含有一种相同元素,且A是一种单质,A会转化成B、D,所以A可能是碳,C会转化成D、B、水,D会转化成碳酸钙,所以D是二氧化碳,B就是一氧化碳,所以C可能是甲烷,碳和充足的氧气反应生成二氧化碳,和不充足的氧气反应生成一氧化碳,甲烷和充足的氧气反应生成二氧化碳和水,和不充足的氧气反应生成一氧化碳和水,水和氧化钙反应生成氢氧化钙,氢氧化钙和二氧化碳会生成碳酸钙,碳酸钙和盐酸反应会生成水,推导正确,所以碳的用途有:还原金属氧化物;
(2)反应③是甲烷生成了一氧化碳,反应④是甲烷生成了二氧化碳,所以最主要区别是:氧气是否充分;
(3)反应⑧是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2;
(4)反应⑥是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
(5)通过分析可知,反应②是碳和充足的氧气反应生成二氧化碳,反应①是碳和不充足的氧气反应生成一氧化碳,反应④是甲烷和充足的氧气反应生成二氧化碳和水,反应③是甲烷和不充足的氧气反应生成一氧化碳和水,反应⑧是水和氧化钙反应生成氢氧化钙,反应⑨是氢氧化钙和二氧化碳会生成碳酸钙,反应⑦是碳酸钙和盐酸反应会生成水、二氧化碳和氯化钙,所以①~⑨中,利用图2所示装置进行试验,能观察到试管中有明显现象有:⑧、⑥、⑦,能观察到的现象的是:有气泡产生、导管内液面上升、紫色石蕊溶液变红色.
故答案为:(1)还原金属氧化物;
(2)氧气是否充分;
(3)CaO+H2O=Ca(OH)2;
(4)CO2+Ca(OH)2=CaCO3↓+H2O;
(6)⑧、⑥、⑦,有气泡产生、导管内液面上升、紫色石蕊溶液变红色.
(2)反应③是甲烷生成了一氧化碳,反应④是甲烷生成了二氧化碳,所以最主要区别是:氧气是否充分;
(3)反应⑧是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2;
(4)反应⑥是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
(5)通过分析可知,反应②是碳和充足的氧气反应生成二氧化碳,反应①是碳和不充足的氧气反应生成一氧化碳,反应④是甲烷和充足的氧气反应生成二氧化碳和水,反应③是甲烷和不充足的氧气反应生成一氧化碳和水,反应⑧是水和氧化钙反应生成氢氧化钙,反应⑨是氢氧化钙和二氧化碳会生成碳酸钙,反应⑦是碳酸钙和盐酸反应会生成水、二氧化碳和氯化钙,所以①~⑨中,利用图2所示装置进行试验,能观察到试管中有明显现象有:⑧、⑥、⑦,能观察到的现象的是:有气泡产生、导管内液面上升、紫色石蕊溶液变红色.
故答案为:(1)还原金属氧化物;
(2)氧气是否充分;
(3)CaO+H2O=Ca(OH)2;
(4)CO2+Ca(OH)2=CaCO3↓+H2O;
(6)⑧、⑥、⑦,有气泡产生、导管内液面上升、紫色石蕊溶液变红色.
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
日常生活中的下列食品富含维生素的是( )
A、 |
B、 |
C、 |
D、 |
由于大气中二氧化碳含量的增加,产生“温室效应”使地球变热,海平面升高,陆地面积减少.为了减少大气中的二氧化碳含量,下列措施可行的是( )
| A、开展植树造林,增强地球表面绿化面积 |
| B、用石灰水吸收空气中的二氧化碳 |
| C、改变能源结构,发展太阳能、核能、水能以代替矿物燃料 |
| D、限制汽车工业发展,减少汽车数量 |








 如图为水通电分解的实验装置图,据图分析:
如图为水通电分解的实验装置图,据图分析: